CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
Tissue macrophages: origin, heterogenity, biological functions, diseases and therapeutic targets

IF=40.8
Abstract
Macrophages are immune cells belonging to the mononuclear phagocyte system. They play crucial roles in immune defense, surveillance, and homeostasis. This review systematically discusses the types of hematopoietic progenitors that give rise to macrophages, including primitive hematopoietic progenitors, erythro-myeloid progenitors, and hematopoietic stem cells. These progenitors have distinct genetic backgrounds and developmental processes. Accordingly, macrophages exhibit complex and diverse functions in the body, including phagocytosis and clearance of cellular debris, antigen presentation, and immune response, regulation of inflammation and cytokine production, tissue remodeling and repair, and multi-level regulatory signaling pathways/crosstalk involved in homeostasis and physiology. Besides, tumor-associated macrophages are a key component of the TME, exhibiting both anti-tumor and pro-tumor properties. Furthermore, the functional status of macrophages is closely linked to the development of various diseases, including cancer, autoimmune disorders, cardiovascular disease, neurodegenerative diseases, metabolic conditions, and trauma. Targeting macrophages has emerged as a promising therapeutic strategy in these contexts. Clinical trials of macrophage-based targeted drugs, macrophage-based immunotherapies, and nanoparticle-based therapy were comprehensively summarized. Potential challenges and future directions in targeting macrophages have also been discussed. Overall, our review highlights the significance of this versatile immune cell in human health and disease, which is expected to inform future research and clinical practice.
摘要
巨噬细胞是属于单核吞噬细胞系统的免疫细胞。它们在免疫防御、监视和稳态中发挥着关键作用。本综述系统地讨论了产生巨噬细胞的造血祖细胞类型,包括原始造血祖细胞、红髓祖细胞和造血干细胞。这些祖细胞具有不同的遗传背景和发育过程。相应地,巨噬细胞在体内表现出复杂多样的功能,包括吞噬和清除细胞碎片、抗原呈递、免疫反应、调节炎症和细胞因子产生、组织重塑和修复,以及参与稳态和生理的多级调节信号通路/相互作用。此外,肿瘤相关巨噬细胞是肿瘤微环境(TME)的关键组成部分,表现出抗肿瘤和促肿瘤的双重特性。此外,巨噬细胞的功能状态与多种疾病的发展密切相关,包括癌症、自身免疫性疾病、心血管疾病、神经退行性疾病、代谢性疾病和创伤。靶向巨噬细胞作为一种有前景的治疗策略在这些背景下应运而生。全面总结了基于巨噬细胞的靶向药物临床试验、基于巨噬细胞的免疫疗法和基于纳米粒子的治疗。还讨论了靶向巨噬细胞的潜在挑战和未来方向。总体而言,我们的综述强调了这种多功能免疫细胞在人类健康和疾病中的重要性,这有望为未来的研究和临床实践提供信息。
总结
1、背景知识
巨噬细胞是单核吞噬细胞系统的一部分,广泛分布于血液和组织中,参与免疫防御、监视和稳态维持。巨噬细胞的起源包括原始造血祖细胞、红-髓系祖细胞(EMPs)和造血干细胞(HSCs)。这些祖细胞具有不同的遗传背景和发育过程,导致巨噬细胞在体内展现出复杂多样的功能。
2、研究方法
文章通过回顾性研究,系统地讨论了巨噬细胞的起源、异质性和极化。研究方法包括对巨噬细胞起源的历史研究、对巨噬细胞在不同疾病中作用的分析,以及对巨噬细胞靶向治疗的临床试验的总结。
3、实验和关键结论
巨噬细胞的起源和异质性:巨噬细胞起源于胚胎时期的EMPs和EMPs衍生的巨噬细胞前体(PreMacs)。这些细胞在特定组织部位迁移和定植,进一步分化成熟。巨噬细胞的身份由其驻留的组织印记,组织特异性转录程序对组织巨噬细胞的维持、表型和功能特征至关重要。
巨噬细胞的生物学功能:巨噬细胞在体内几乎所有的生物学过程中都扮演着复杂多样的角色,包括吞噬和清除细胞碎片、抗原呈递、免疫反应调节、炎症和细胞因子产生、组织重塑和修复等。
巨噬细胞在疾病中的作用:巨噬细胞的功能状态与多种疾病的发展密切相关,包括癌症、自身免疫性疾病、心血管疾病、神经退行性疾病、代谢性疾病和创伤等。例如,在肿瘤微环境中,肿瘤相关巨噬细胞(TAMs)表现出促肿瘤和抗肿瘤的双重特性。
巨噬细胞作为治疗靶点:随着技术的发展,如基因编辑、纳米药物递送系统等,针对巨噬细胞的治疗策略已成为一种有前景的治疗手段。文章总结了巨噬细胞靶向药物、巨噬细胞免疫疗法和纳米粒子治疗的临床试验。巨噬细胞可以内化和运输药物、纳米颗粒或基因治疗载体至靶组织,促进局部药物递送。这种方法可以通过增加疾病部位的药物积累并减少非靶效应来提高治疗指数。特别是,自体或异体巨噬细胞可以在体外工程化或极化后给患者使用。这些基于巨噬细胞的细胞疗法可以补充或替代功能失调的巨噬细胞,调节免疫反应,或促进组织再生。方法包括在重新引入体内之前体外极化巨噬细胞以增强其再生特性。这在治疗心肌梗死和慢性伤口等需要促进组织修复的疾病中具有重要意义。
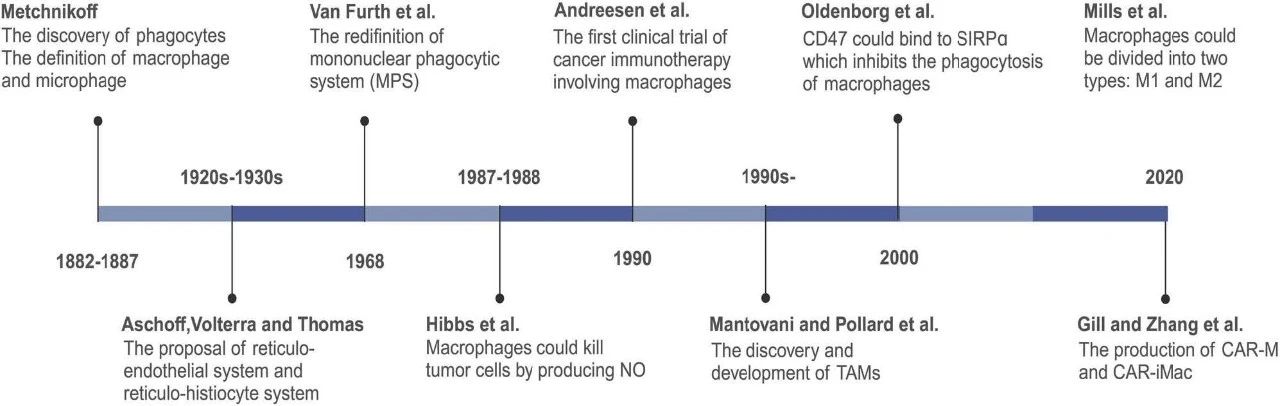
图 1:巨噬细胞研究的历史与里程碑事件时间线。
NO:一氧化氮,TAMs:肿瘤相关巨噬细胞,CAR-M:嵌合抗原受体巨噬细胞,CAR-iMac:由诱导多能干细胞(iPSCs)衍生的嵌合抗原受体表达巨噬细胞。
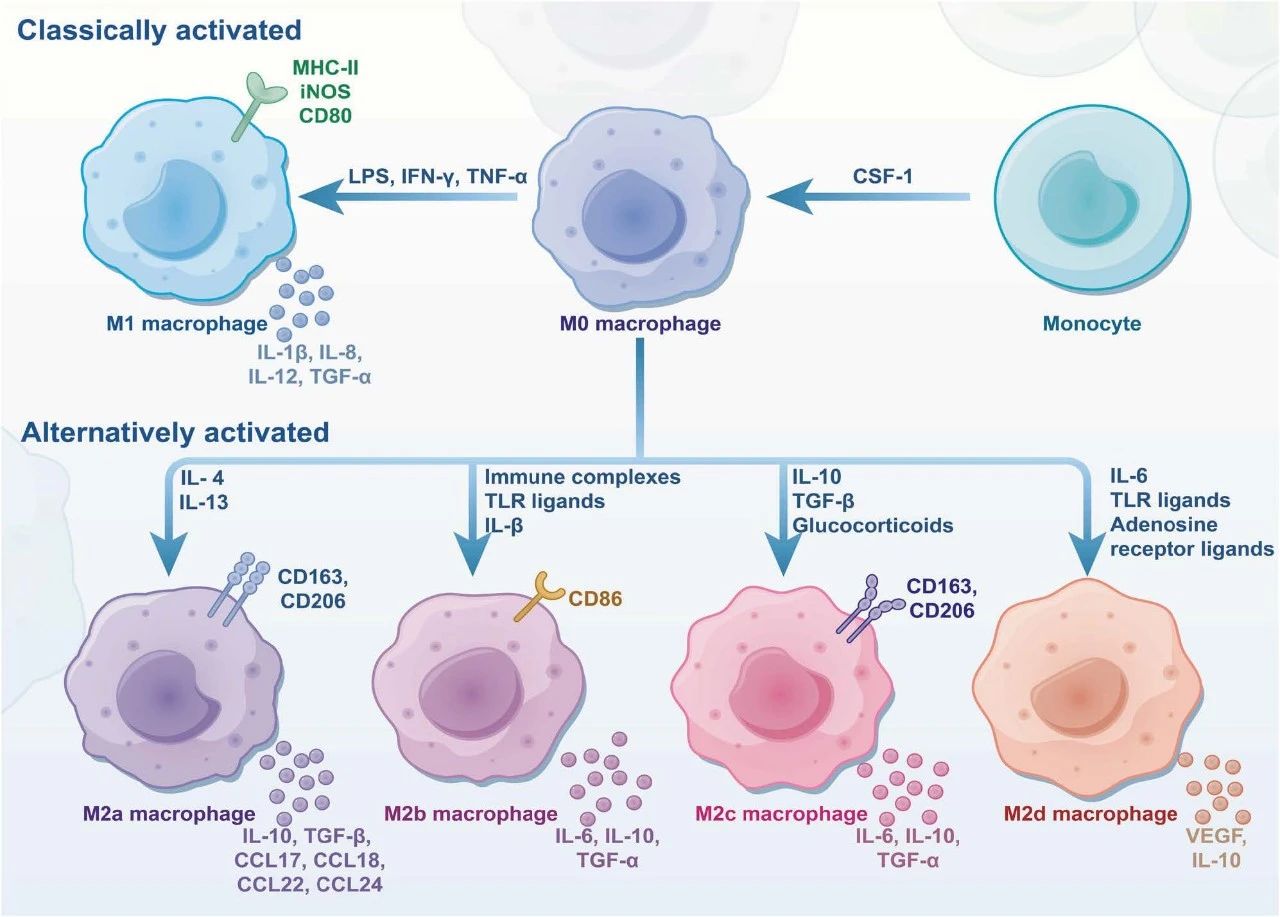
图 2:CSF-1 可诱导单核细胞分化为 M0 巨噬细胞。
M0 巨噬细胞在 Th1 型或 Th2 型细胞因子的刺激下,进一步分化为 M1 或 M2 巨噬细胞。M2 巨噬细胞根据激活模式和其他特征可进一步细分为四个亚型:M2a、M2b、M2c 和 M2d。不同类型的巨噬细胞表达不同的分子标记,并分泌不同的物质,在多种生理和病理过程中发挥重要作用。
CSF-1:集落刺激因子-1,MHC-II:主要组织相容性复合体 II 类,iNOS:诱导型一氧化氮合酶,LPS:脂多糖,IFN-γ:干扰素-γ,TNF-α:肿瘤坏死因子-α,IL-1β:白细胞介素-1β,IL-8:白细胞介素-8,IL-12:白细胞介素-12。
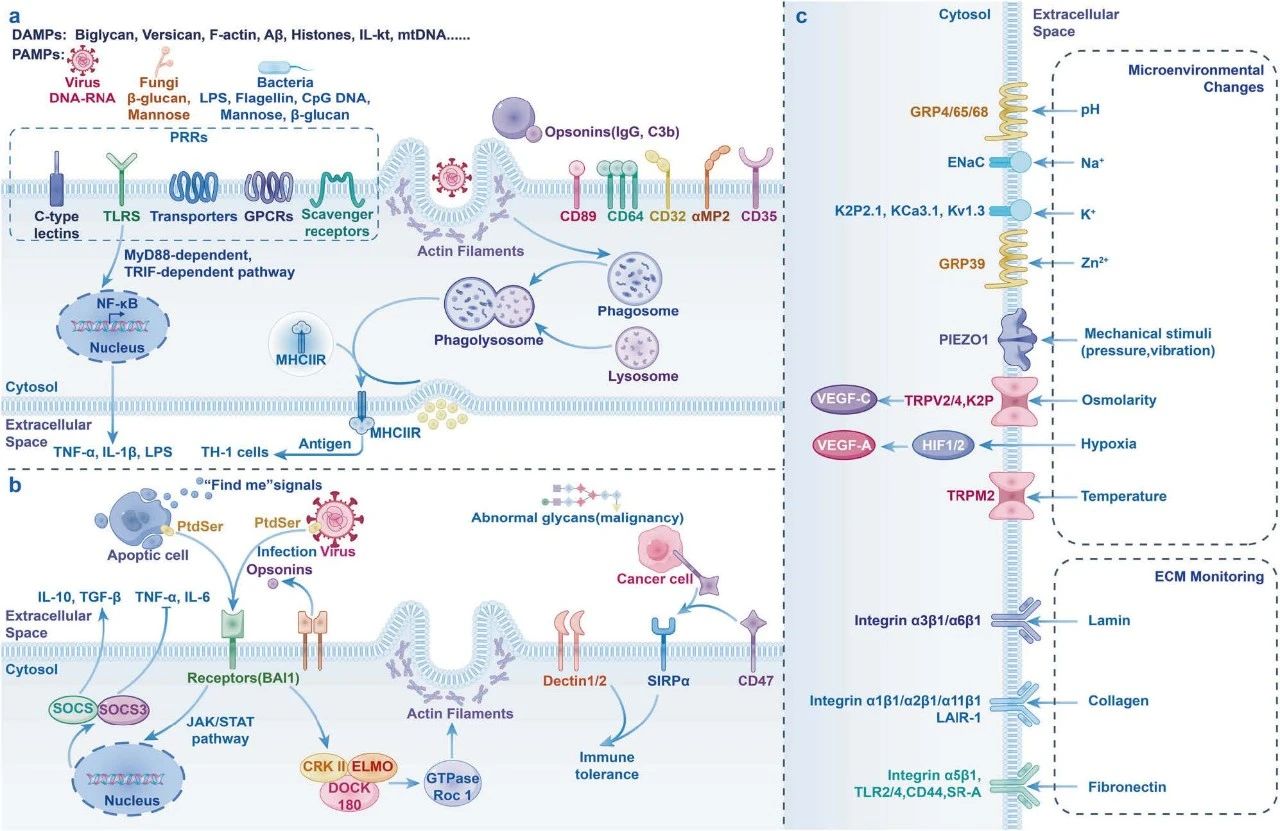
图 3:TRMs 在炎症和稳态中的作用。
1. 典型的促炎反应由模式识别受体(PRRs)或调理素受体启动。PRRs 可以直接识别损伤相关分子模式(DAMPs)和病原体相关分子模式(PAMPs)。调理素受体介导的识别过程涉及与调理素标记的外来颗粒及调理素受体(如 Fcγ 受体)的结合,进而激活肌动蛋白聚合、促炎细胞因子释放等反应。吞噬体与溶酶体融合,MHC-II 分子通过 HLA-DM 依赖机制装载抗原,并递送至质膜,刺激抗原特异性 CD4+ T 细胞。
2. 炎症的消退过程。凋亡细胞通过释放“来找我”信号(如 ATP、溶血磷脂胆碱、CX3CL1)招募肿瘤相关巨噬细胞(TAMs)。吞噬作用通过受体与凋亡细胞上的“吃我”信号结合,或通过桥接分子(如 MFGE8、C1q 等)间接识别,进一步激活免疫消退细胞因子。
3. TRMs 感应微环境中的物理因素。
SIRPα:信号调节蛋白α,LPC:溶血磷脂胆碱,PRRs:模式识别受体,PAMPs:病原体相关分子模式,DAMPs:损伤相关分子模式,MIIC:MHC-II 类小室,LPS:脂多糖,HLA:人类白细胞抗原。
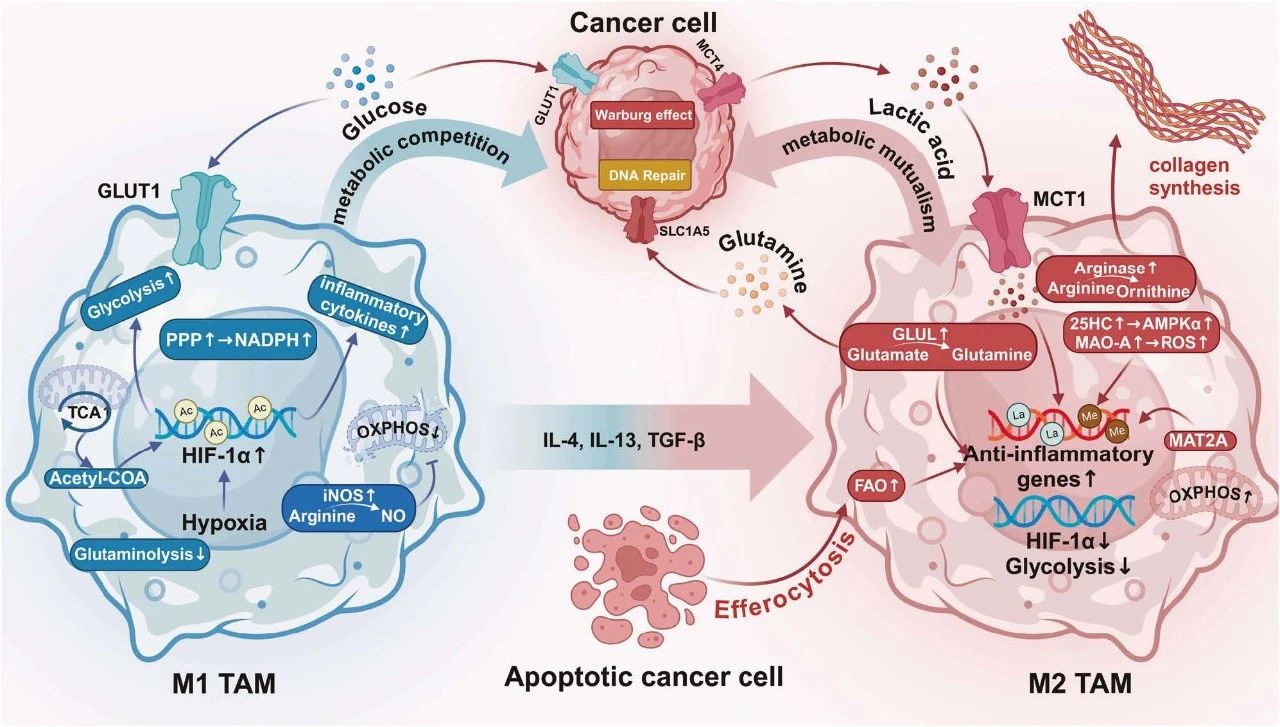
图 4:M1 和 M2 巨噬细胞之间的代谢差异。
在肿瘤微环境中,M1 巨噬细胞和癌细胞的代谢差异与癌症的发生和发展密切相关。M1 巨噬细胞和癌细胞主要依赖糖酵解,导致代谢竞争。随着肿瘤恶性程度的进展,M1 巨噬细胞逐渐重编程为 M2 型,代谢转向氧化磷酸化。M2 巨噬细胞与癌细胞之间的代谢产物交换,进一步促进肿瘤的生物学特性。这一过程突出了肿瘤微环境的复杂性,强调了巨噬细胞在肿瘤发展中的关键作用。
ppp:戊糖磷酸途径,NADPH:还原型烟酰胺腺嘌呤二核苷酸磷酸,HIF-1α:缺氧诱导因子-1α,OXPHOS:氧化磷酸化,GLUT1:葡萄糖转运蛋白 1,MCT4:单羧酸转运蛋白 4,MCT1:单羧酸转运蛋白 1,SLC1A5:溶质载体家族 1 成员 5,IL-4:白细胞介素-4,IL-13:白细胞介素-13,TGF-β:转化生长因子-β,FAO:脂肪酸氧化,25HC:25-羟基胆固醇,AMPKα:AMPK α 亚基,MAO-A:单胺氧化酶 A,ROS:活性氧,MAT2A:甲硫氨酸腺苷基转移酶 2A。
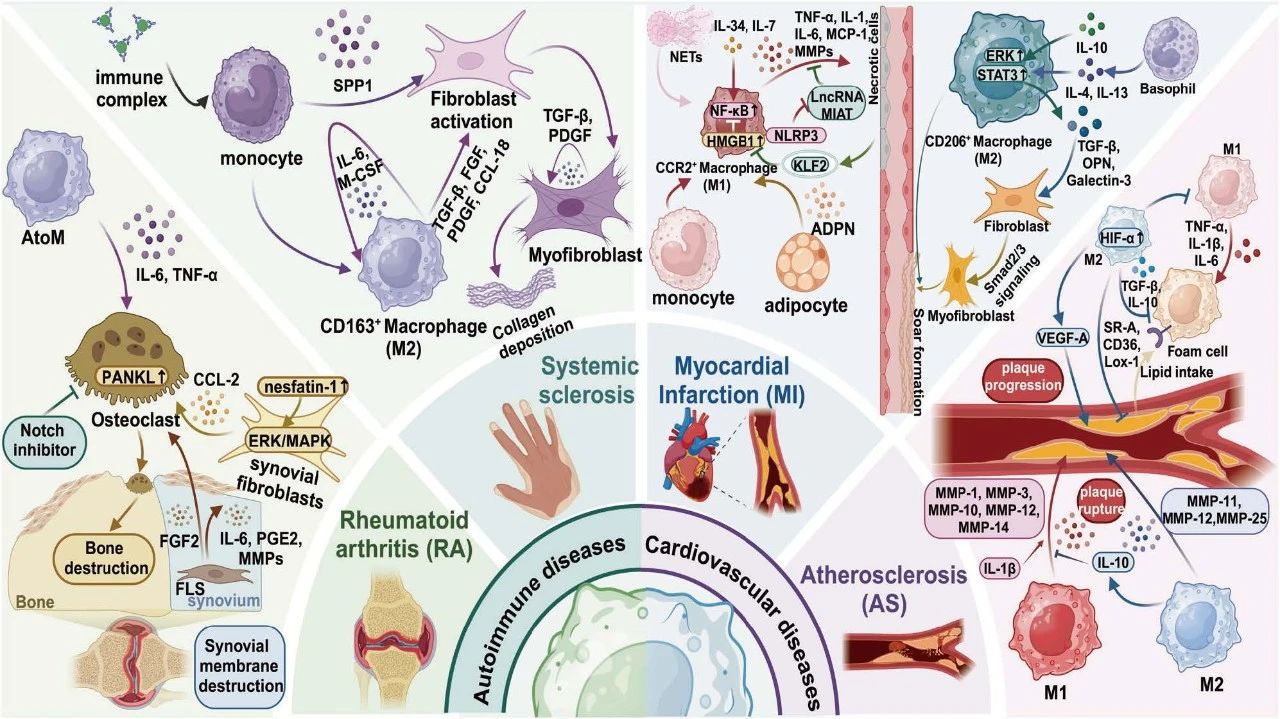
图 5:组织巨噬细胞在疾病中的作用。
在类风湿关节炎和系统性硬化症等自身免疫疾病中,巨噬细胞通过释放促炎细胞因子(如 IL-6 和 TNF-α)引起组织损伤,并通过抗炎和纤维化因子促进多组织纤维化。在心血管疾病中(如动脉粥样硬化和心肌梗死),巨噬细胞的极化作用促进坏死组织的吞噬、纤维化修复、心肌重塑以及动脉粥样硬化斑块的形成和破裂。
AtoM:关节炎相关破骨细胞前体巨噬细胞,IL-6:白细胞介素-6,TNF-α:肿瘤坏死因子-α,PANKL:甲状旁腺激素相关蛋白,CCL2:化学趋化因子配体 2,ERK:细胞外信号调节激酶,MAPK:丝裂原活化蛋白激酶,FGF2:纤维细胞生长因子 2,PGE2:前列腺素 E2,SPP1:分泌磷蛋白 1,TGF-β:转化生长因子-β,PDGF:血小板衍生生长因子,CCL-18:化学趋化因子配体 18,IL-34:白细胞介素-34,IL-7:白细胞介素-7,IL-1:白细胞介素-1,MCP-1:单核细胞趋化蛋白-1,NLRP3:NOD 样受体蛋白 3,KLF2:Krüppel 样因子 2,ADPN:脂联素,NF-κB:核因子 κB,HMGB1:高迁移率族蛋白 B1,IL-4:白细胞介素-4,IL-13:白细胞介素-13,OPN:骨桥蛋白,HIF-α:缺氧诱导因子α。
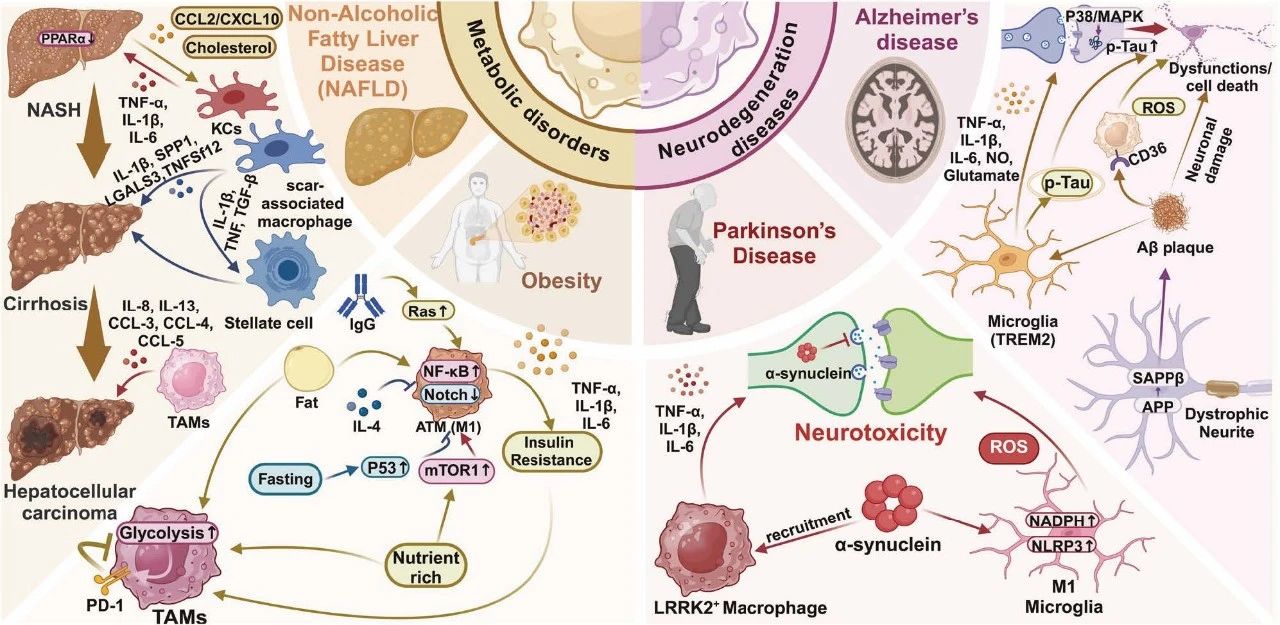
图 6:组织巨噬细胞在疾病中的作用。
在阿尔茨海默病和帕金森病等神经退行性疾病中,巨噬细胞参与神经元损伤和神经毒性,涉及淀粉样蛋白-β 和 α-突触核蛋白的处理。在代谢紊乱中,肥胖作为一种全身性慢性炎症状态,巨噬细胞通过与肿瘤相关巨噬细胞的相互作用加速胰岛素抵抗的发生,并影响基于细胞的免疫治疗效果。此外,巨噬细胞还在肝病的进展中发挥多重功能,包括肝炎、肝硬化和肝细胞癌。
p-Tau:磷酸化 tau,APP:淀粉样前体蛋白,SAPPβ:可溶性淀粉样前体蛋白β,TREM2:触发受体表达于髓样细胞 2,LRRK2:富亮氨酸重复激酶 2,NADPH:还原型烟酰胺腺嘌呤二核苷酸磷酸,NOTCH:Notch 信号通路,mTOR1:机械靶蛋白复合体 1。