IF=39.3!高分综述讨论抗铁死亡的治疗策略!
In defence of ferroptosis
IF=39.3!高分综述讨论抗铁死亡的治疗策略!
In defence of ferroptosis
From: Signal Transduction and Targeted Therapy,IF=39.3。
Abstract
Rampant phospholipid peroxidation initiated by iron causes ferroptosis unless this is restrained by cellular defences. Ferroptosis is increasingly implicated in a host of diseases, and unlike other cell death programs the physiological initiation of ferroptosis is conceived to occur not by an endogenous executioner, but by the withdrawal of cellular guardians that otherwise constantly oppose ferroptosis induction. Here, we profile key ferroptotic defence strategies including iron regulation, phospholipid modulation and enzymes and metabolite systems: glutathione reductase (GR), Ferroptosis suppressor protein 1 (FSP1), NAD(P)H Quinone Dehydrogenase 1 (NQO1), Dihydrofolate reductase (DHFR), retinal reductases and retinal dehydrogenases (RD) and thioredoxin reductases (TR). A common thread uniting all key enzymes and metabolites that combat lipid peroxidation during ferroptosis is a dependence on a key cellular reductant, nicotinamide adenine dinucleotide phosphate (NADPH). We will outline how cells control central carbon metabolism to produce NADPH and necessary precursors to defend against ferroptosis. Subsequently we will discuss evidence for ferroptosis and NADPH dysregulation in different disease contexts including glucose-6-phosphate dehydrogenase deficiency, cancer and neurodegeneration. Finally, we discuss several anti-ferroptosis therapeutic strategies spanning the use of radical trapping agents, iron modulation and glutathione dependent redox support and highlight the current landscape of clinical trials focusing on ferroptosis.
摘要
如果没有防御机制的抑制,细胞可能会发生由铁引发的脂质过氧化所驱动的细胞铁死亡(ferroptosis)。铁死亡与多种疾病的关系受到越来越多的关注。与其他细胞死亡程序不同,铁死亡的生理启动并非由内源性执行因子引发,而是因为细胞中持续抑制铁死亡的诱导的保护因子的缺失而引发。在本文中,我们对关键的铁死亡防御策略进行了剖析,包括铁的调节、磷脂的修饰以及酶和代谢物系统:谷胱甘肽还原酶(GR)、铁死亡抑制蛋白1(FSP1)、NAD(P)H醌还原酶1(NQO1)、二氢叶酸还原酶(DHFR)、视黄醇还原酶和视黄醛脱氢酶(RDH)以及硫氧还蛋白还原酶(TR)。所有这些对抗铁死亡过程中脂质过氧化的关键酶和代谢物都有一个共同点,即依赖一种关键的细胞还原剂——烟酰胺腺嘌呤二核苷酸磷酸(NADPH)。我们将阐述细胞如何调控中心碳代谢以产生NADPH和必要的前体物质来抵御铁死亡。接下来我们讨论了铁死亡和NADPH失调在不同疾病背景下的证据,包括葡萄糖-6-磷酸脱氢酶缺乏症、癌症和神经退行性疾病。文章最后我们讨论了几种抗铁死亡的治疗策略,包括自由基捕获剂的使用、铁的调节和谷胱甘肽依赖的氧化还原支持,并概述了当前聚焦于铁死亡的临床试验的现状。
内容总结
01 研究背景
铁死亡的定义:铁死亡是一种由铁离子催化的磷脂过氧化引起的细胞死亡方式,除非被细胞防御机制抑制,否则会导致细胞破裂。
铁死亡与疾病的关系:铁死亡与多种疾病相关,其生理启动方式与其他细胞死亡程序不同,通常是由细胞抗氧化防御机制的缺失引发的。
02 铁死亡的关键防御策略
铁调节:细胞通过多种储存、运输和出口蛋白(如铁蛋白、转铁蛋白、肝素、铁蛋白和转铁蛋白受体1)严格调控铁水平,以避免过量铁产生的活性氧(ROS)。
磷脂调节:磷脂过氧化是铁死亡的执行者,磷脂的组成决定了细胞对铁死亡的敏感性。
酶和代谢物系统:包括谷胱甘肽还原酶(GR)、铁死亡抑制蛋白1(FSP1)、NAD(P)H醌还原酶1(NQO1)、二氢叶酸还原酶(DHFR)、视黄醇还原酶和视黄醛脱氢酶(RDH)以及硫氧还蛋白还原酶(TR)。这些酶和代谢物依赖于关键的细胞还原剂——烟酰胺腺嘌呤二核苷酸磷酸(NADPH)。
03 铁死亡的模型和实验方法
体外模型:通过抑制系统xc-(如使用erastin或谷氨酸)、抑制谷胱甘肽合成(如使用buthionine sulphoximine, BSO)、直接或间接抑制GPX4(如使用RSL3、FIN56或FINO2)以及增加铁依赖性脂质过氧化来诱导铁死亡。
体内模型:目前缺乏特定的铁死亡抑制剂或激活剂被批准用于临床,且缺乏特定的生物标志物来测量体内铁死亡。
04 铁死亡涉及的细胞器
线粒体、内质网和高尔基体:这些细胞器的磷脂膜结合的铁死亡可以通过过度脂质过氧化被引发和传播。
过氧化物酶体:可能不仅是脂质过氧化的场所,也是传播铁死亡所必需的脂质过氧化的载体。
脂滴:通过增加脂滴的数量和大小来隔离和保护PUFA免受过氧化,从而保护细胞免受铁死亡。
细胞核和溶酶体:细胞核通过调节抗氧化防御系统来调节铁死亡,而溶酶体则通过多种机制(如自噬依赖的铁蛋白降解)调节铁死亡。
05 磷脂过氧化与铁死亡的敏感性
磷脂组成:细胞膜磷脂的组成决定了细胞对铁死亡的敏感性,特别是磷脂酰乙醇胺(PE)和磷脂酰丝氨酸(PS)的氧化。
磷脂重塑:通过Lands循环,磷脂可以选择性地替换酰基链,从而调节磷脂对铁死亡的敏感性。
06 铁在铁死亡中的作用
铁的化学性质:铁的氧化还原循环特性使其在细胞功能中至关重要,但也可能导致氧化应激和脂质过氧化。
铁的调节:细胞通过铁蛋白储存铁,通过转铁蛋白受体1(TFR1)控制铁的流入,通过铁蛋白(FPN1)控制铁的流出,以避免过量铁引起的铁死亡。
07 铁死亡防御中的酶代谢耦合
NADPH的作用:NADPH是铁死亡防御的关键代谢物,为多种抗氧化酶提供还原力。
关键酶和代谢物:包括谷胱甘肽还原酶(GR)、铁死亡抑制蛋白1(FSP1)、NAD(P)H醌还原酶1(NQO1)、二氢叶酸还原酶(DHFR)、视黄醇还原酶和硫氧还蛋白还原酶(TR)。
08 铁死亡与疾病的关系
葡萄糖-6-磷酸脱氢酶(G6PD)缺乏症:G6PD是PPP途径中的关键酶,其缺乏会导致NADPH生成减少,增加铁死亡的敏感性。
癌症:癌细胞通过代谢重编程增加PPP途径的活性,以产生更多的NADPH,从而增强抗氧化防御。
神经退行性疾病:包括阿尔茨海默病、帕金森病和亨廷顿病,这些疾病中观察到铁积累、脂质过氧化和抗氧化防御系统受损,提示铁死亡可能在这些疾病中起作用。
09 铁死亡的治疗策略
自由基捕获剂(RTAs):如铁死亡抑制剂(ferrostatin-1)和脂氧素抑制剂(liproxstatin-1)。
铁调节:通过铁螯合剂(如去铁胺)减少铁的可用性。
谷胱甘肽依赖的氧化还原支持:通过补充谷胱甘肽或其前体来增强抗氧化防御。
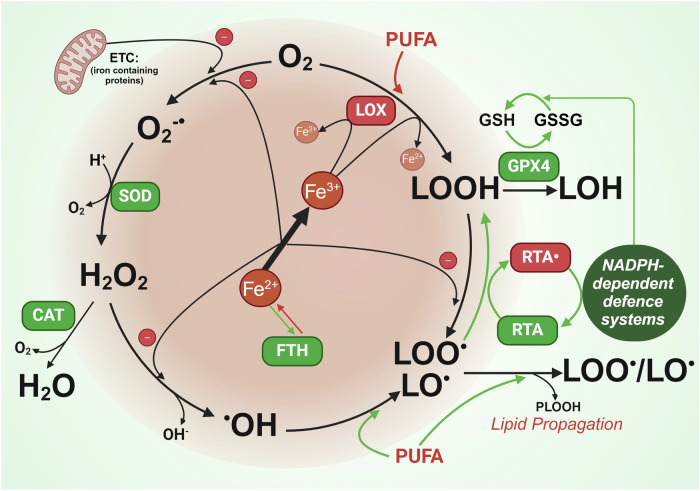
图1. 铁在活性氧生成和脂质过氧化中的核心作用。
铁直接和间接地在多个点上产生活性氧和脂质过氧化。间接地,电子传递链中的含铁蛋白产生超氧阴离子(O2-),超氧歧化酶(SOD)将其还原为过氧化氢(H2O2)。过氧化氢可以被过氧化氢酶(CAT)清除,也可以与铁发生芬顿反应,生成羟基自由基(•OH)。芬顿反应还可以催化脂质过氧化氢(LOOH)生成脂质过氧自由基(LOO• /LO•)。自由基捕获剂(RTAs)可以清除脂质过氧自由基。间接地,含铁的脂氧合酶(LOX)催化多不饱和脂肪酸(PUFAs)和脂质的氧化,产生脂质过氧化氢(LOOH)。谷胱甘肽过氧化物酶4(GPX4)可以通过将脂质过氧化氢(PLOOH,高铁死亡风险)还原为无害的脂质醇(LOH),从而阻止脂质过氧化和传播。GPX4的还原能力依赖于还原型谷胱甘肽(GSH),而GSH依赖于NADPH将其还原型谷胱甘肽二硫化物(GSSG)回收。铁储存蛋白铁蛋白(FTH)的分解可能导致游离铁增加,从而促进这些反应。
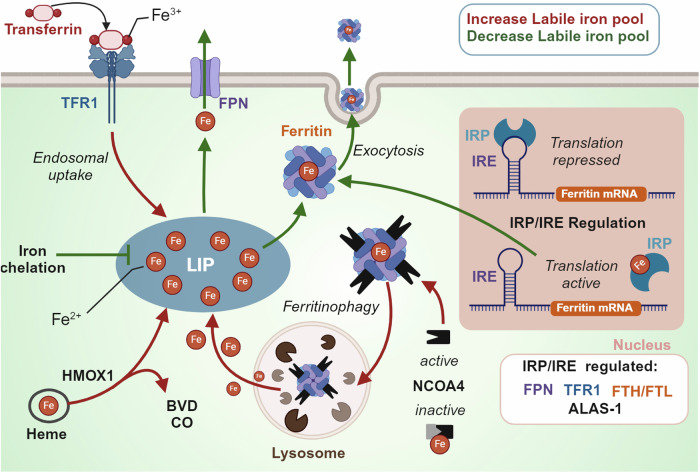
图2. 细胞内游离铁池的调节。
游离铁池由多种蛋白质调节,包括:
i) 转铁蛋白受体1(TFR1),它促进以转铁蛋白形式的铁摄入;
ii) 铁输出蛋白(FPN),一种促进铁输出的铁通道;
iii) 铁蛋白,它可以储存游离铁或在溶酶体降解后释放铁,这一过程由核受体激活因子4(NCOA4)介导;
iv) 血红素降解,由血红素氧合酶1(HMOX-1)介导,释放铁并产生胆绿素(BVD)和一氧化碳(CO)。铁反应蛋白/铁反应元件(IRP/IRE)系统对游离铁浓度做出反应,并随后调节多种参与铁调节的蛋白质的表达。
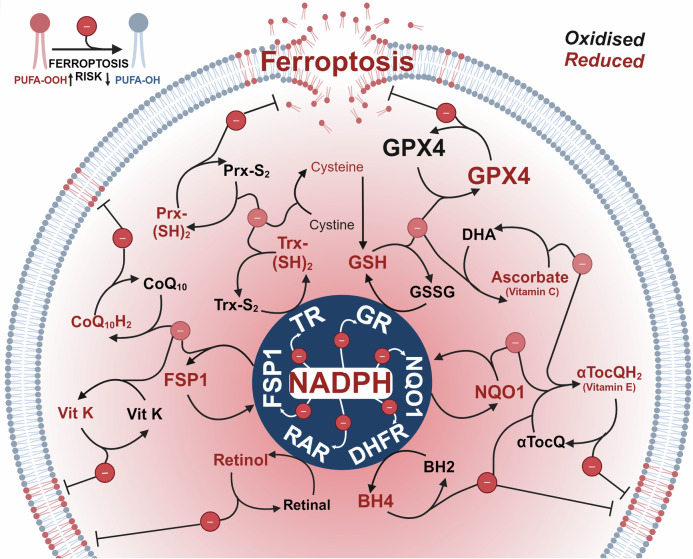
图3. NADPH的还原力为铁死亡防御提供动力。
每个烟酰胺腺嘌呤二核苷酸磷酸(NADPH)分子可以捐赠两个电子。NADPH捐赠的电子可以还原关键的抗铁死亡酶,包括谷胱甘肽还原酶(GR)、铁死亡抑制蛋白1(FSP1)、NAD(P)H醌还原酶1(NQO1)、二氢叶酸还原酶(DHFR)以及视网膜脱氢酶(RDH)和硫氧还蛋白还原酶(TR),这些酶能够进一步促进多种代谢物和蛋白质的还原反应,包括视黄醇、视黄醛、四氢生物蝶呤(BH4)、二氢生物蝶呤(BH2)、α-生育酚醌(αTocQ)、α-生育酚醌醇(αTocQH2)、抗坏血酸、脱氢抗坏血酸(DHA)、谷胱甘肽(GSH)、谷胱甘肽二硫化物(GSSG)、谷胱甘肽过氧化物酶4(GPX4)、氧化型硫氧还蛋白(Trx-S2)、还原型硫氧还蛋白(Trx-(SH)2)、氧化型过氧化还原酶(Prx-S2)、还原型过氧化还原酶(Prx-(SH)2)、辅酶Q10(CoQ10)、还原型辅酶Q10(CoQ10H2)和维生素K(vit K),最终导致脂质过氧化的预防。
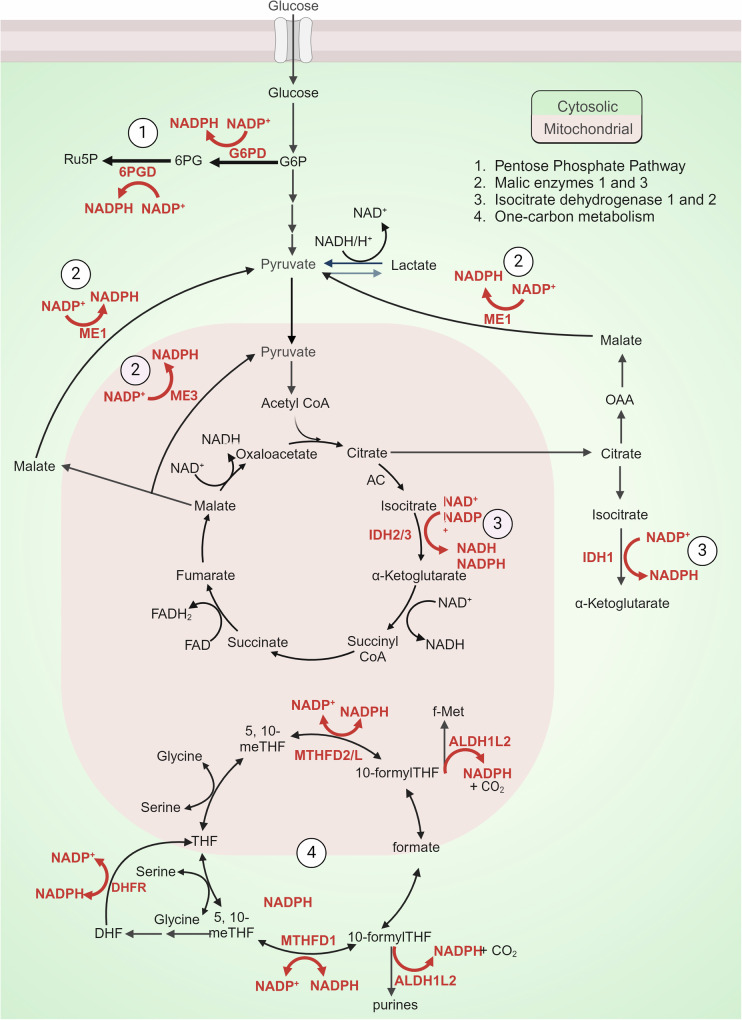
图4. 促进NADPH生成的关键代谢途径。
1) 戊糖磷酸途径,从葡萄糖-6-磷酸(G6P)分流,通过两个脱氢酶步骤再生两个烟酰胺腺嘌呤二核苷酸磷酸(NADPH):i. 通过葡萄糖-6-磷酸脱氢酶(G6PD)将G6P转化为6-磷酸葡萄糖酸(6PG);ii. 通过6-磷酸葡萄糖酸脱氢酶(6PGD)将6PG转化为核糖-5-磷酸(Ru5P)。
2) 位于细胞质(ME1)和线粒体(ME2和ME3)的苹果酸酶1、2和3,催化苹果酸的氧化脱羧反应,生成丙酮酸,同时从NADP生成NADPH。
3) 异柠檬酸脱氢酶(IDHs)催化氧化脱羧反应以产生NADPH。IDH1在细胞质中的分布程度不同,而IDH2/3定位于线粒体。
4) 一碳(1C)和叶酸代谢,涉及一系列1C转化,产生和消耗氧化还原当量,包括通过细胞质(1)/线粒体(2)10-甲酰四氢叶酸脱氢酶(ALDH1L1/2)将10-甲酰-THF氧化为二氧化碳(CO2)。NADPH也可以通过甲基四氢叶酸脱氢酶(MTHFDs)催化的5,10-甲基四氢叶酸与10-甲酰四氢叶酸的可逆转化产生。
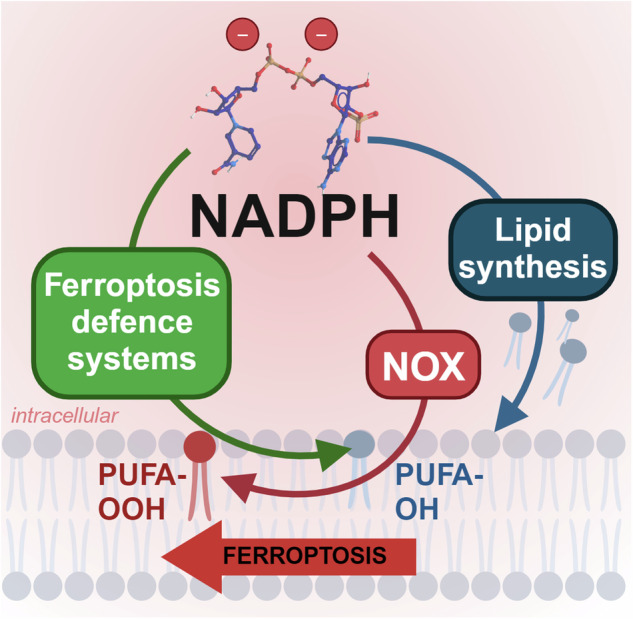
图5. NADPH在铁死亡中的双重作用。
NADPH促进磷脂合成用于磷脂生产,并被含血红素的NADPH氧化酶(NOXs)等酶利用,这些酶将细胞质中的NADPH的电子转移以产生ROS,从而促进脂质过氧化(PUFA-OOH)。然而,NADPH也被抗铁死亡酶招募,以防止脂质过氧化并生成抗铁死亡的磷脂(PUFA-OH)。在稳态中,NADPH对铁死亡防御的招募似乎是主导的,可能用于抑制其促进的促铁死亡途径。
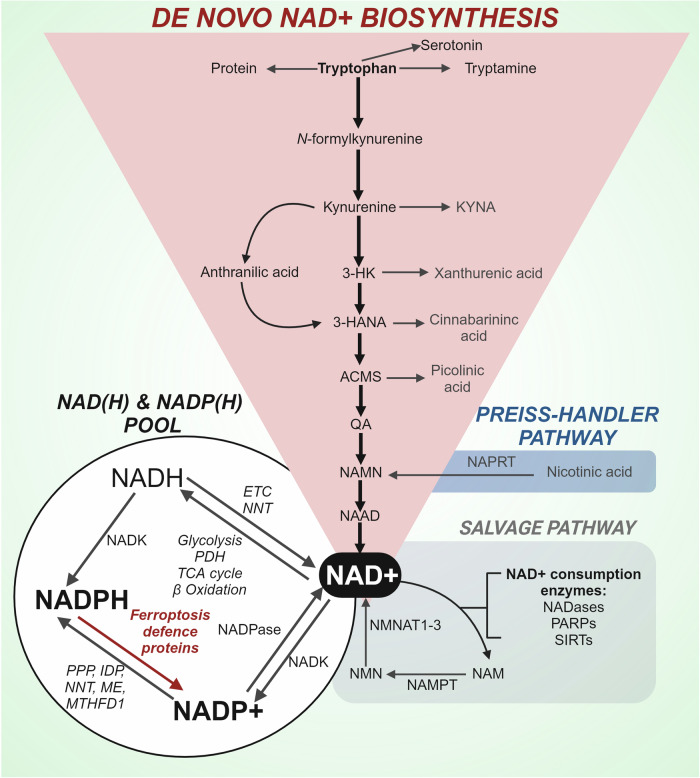
图6. NAD(P)H库以及NAD⁺的代谢。
哺乳动物细胞利用饮食中的色氨酸通过犬尿氨酸途径合成烟酰胺腺嘌呤二核苷酸(NAD⁺)。犬尿氨酸途径有两个关键分支,主要路径优先将犬尿氨酸转化为3 - 羟基犬尿氨酸(3 - HK),然后是3 - 羟基邻氨基苯甲酸(4 - HANA)、2 - 氨基 - 3 - 羧基 - 穆康酸 - 6 - 半醛(ACMS)和喹啉酸(QA),后者转化为烟酰胺单核苷酸(NAMN),这是Preiss - Handler途径的共同中间体。NAMN随后代谢为烟酰胺腺嘌呤二核苷酸(NAAD),这是NAD⁺的直接前体。包括NAD酶、聚(ADP - 核糖)聚合酶(PARPs)和去乙酰化酶(SIRTs)在内的几种酶以NAD⁺为底物,并生成烟酰胺(NAM)。补救途径从NAM前体再生NAD⁺,NAM首先被烟酰胺磷酸核糖转移酶(NAMPT)转化为烟酰胺单核苷酸(NMN),然后通过烟酰胺单核苷酸腺苷基转移酶1 - 3(NMNAT 1 - 3)转化为NAD⁺。NAD⁺通过几种代谢途径和酶贡献于NAD(H)和NADP(H)库;TCA循环,三羧酸循环;ETC,电子传递链;NNT,烟酰胺核苷酸转氢酶;NADK,NAD激酶;PPP,磷酸戊糖途径;IDP,异柠檬酸脱氢酶;ME,苹果酸酶;MTHFD1,亚甲基四氢叶酸脱氢酶;NAPRT,烟酸磷酸核糖转移酶。
参考文献:Alves F, Lane D, Nguyen TPM, Bush AI, Ayton S. In defence of ferroptosis. Signal Transduct Target Ther. 2025 Jan 3;10(1):2. doi: 10.1038/s41392-024-02088-5. PMID: 39746918; PMCID: PMC11696223.
潮新(南京)生物科技有限公司
CHAOXIN (NANJING) BIOTECHNOLOGY CO.,LTD.
联系热线:177-0516-3098
咨询邮箱:sales@chaoxinbio.com
公司地址:南京市栖霞区红枫科技园C3区3楼
官网网址:http://www.chaoxinbio.com