CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
本方法用于建立小鼠心肌缺血再灌注损伤模型,以左前降支(LAD)可逆阻断模拟短暂缺血后再通。流程以异氟烷吸入麻醉、实时心电监测与体温维持为基础,通过缺血期心肌颜色改变及心电ST段变化进行过程质控,并在再灌注后按研究终点开展组织学与功能学评估。
小鼠:雄性C57BL/6J,5–6周龄,体重约20±1g。
饲养:22–25°C,湿度55%±5%,12h光暗循环。
异氟烷麻醉系统(麻醉箱+面罩)+气体流量控制(建议0.5L/min)。
动物心电监护(ECG)系统,用于记录基线与缺血/再灌注判定。
加热垫/保温系统,用于围术期体温维持。
基础外科操作平台与固定带/医用胶带(四肢固定)。
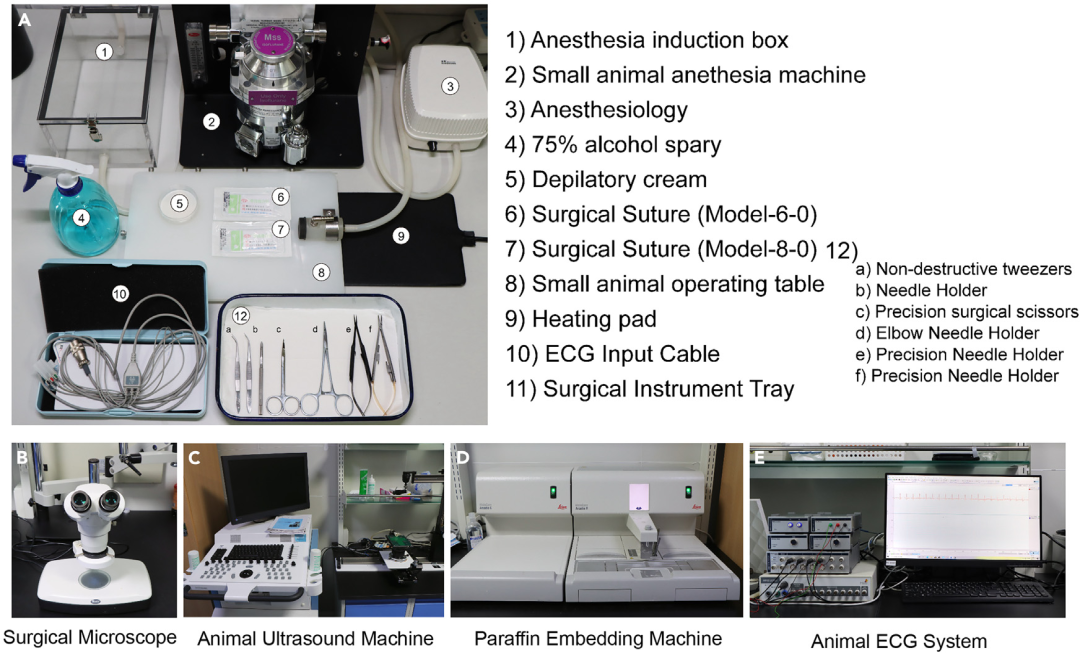
图1. 小鼠心肌梗死与心肌缺血再灌注损伤模型的设备搭建
显微手术器械:剪、镊、持针器、止血钳等。
缝合线:8-0丝线或摩擦力较高的结扎线(用于活结/滑结阻断LAD)。
脱毛膏(约0.5–1g/只,覆盖胸部手术区并向外扩展至少50%)。
消毒用品:0.1%苯扎氯铵(器械浸泡10min后充分晾干)。
麻醉箱预充异氟烷约1min。
诱导麻醉:异氟烷5%,流量0.5L/min;以翻正反射消失为麻醉到位标准,诱导暴露时间建议≤3min。
维持麻醉:异氟烷3%,流量0.5L/min;置于手术板并佩戴与麻醉系统连接的呼吸面罩,确保密封良好。
四肢固定:用医用胶带固定四肢,避免术中移动。
监护与保温:连接ECG获取稳定基线;持续监测呼吸深度与频率;使用加热垫维持体温。若呼吸频率<40次/分钟或出现呼吸暂停,立即下调异氟烷浓度并必要时进行辅助通气。
脱毛:在胸部涂抹脱毛膏(约0.5–1g),覆盖范围较计划切口向外扩展至少50%,按说明去除毛发并清洁。
皮肤消毒与铺巾:常规外科消毒后无菌铺巾。
器械消毒:器械0.1%苯扎氯铵浸泡10min后充分晾干再使用。
开胸:沿肋间隙切开皮肤与肌层,进入胸腔并暴露心脏。
定位LAD:以左心耳为主要解剖标志,LAD通常位于左心耳下方约1–2mm并沿心前壁走行;定位高度应在批内尽量一致以减少危险区(AAR)差异。
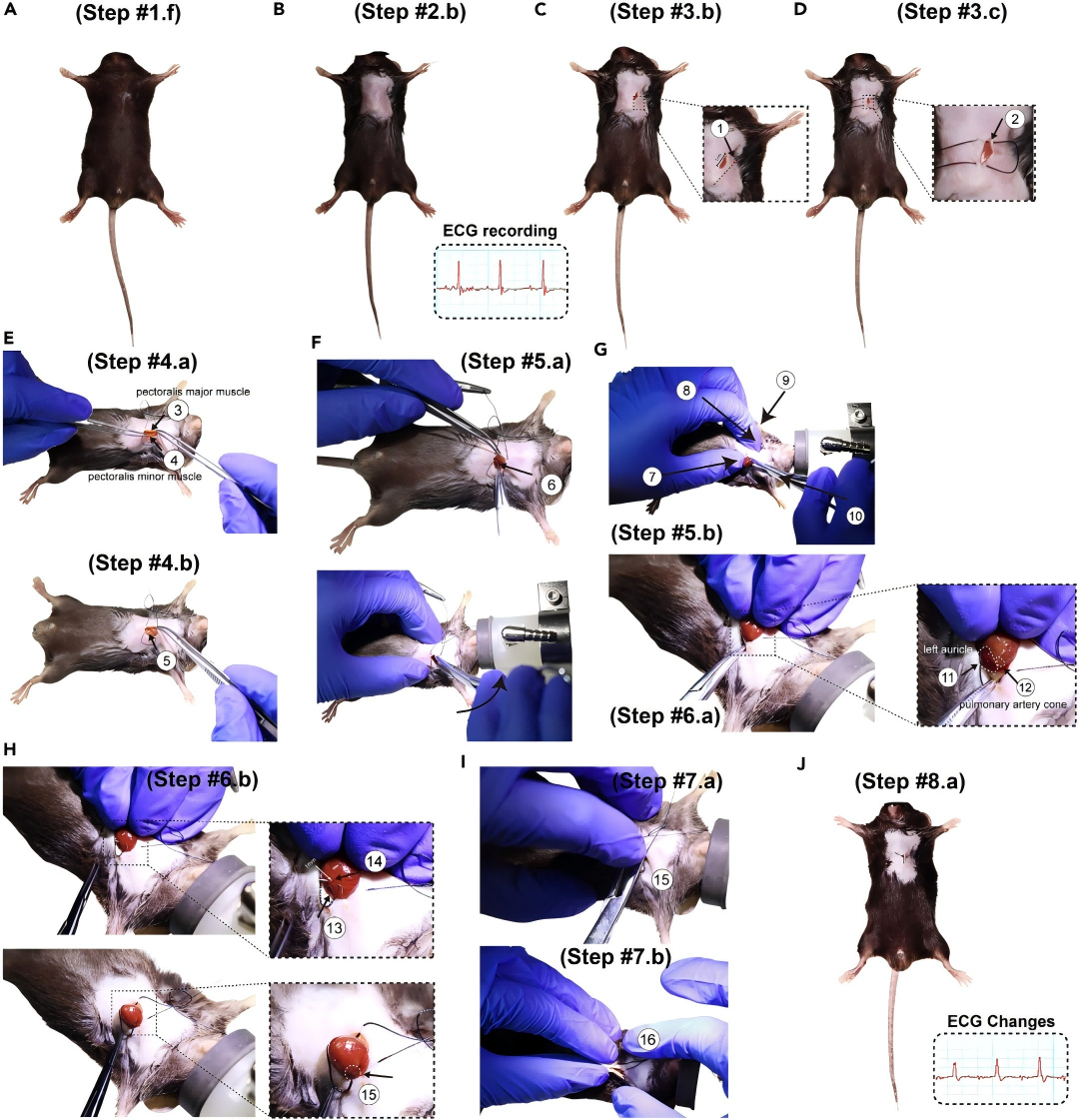
图2. 心肌梗死模型制备的详细流程图
以8-0缝合线在预定位置对LAD行活结/滑结阻断。
缺血判定:左室前壁出现苍白改变,并伴随ECG异常(如ST段抬高、T波改变)。
关闭胸腔后开始计时缺血(常用参数:30min;具体按课题需要设定),缺血期持续观察ECG以确认缺血状态稳定。
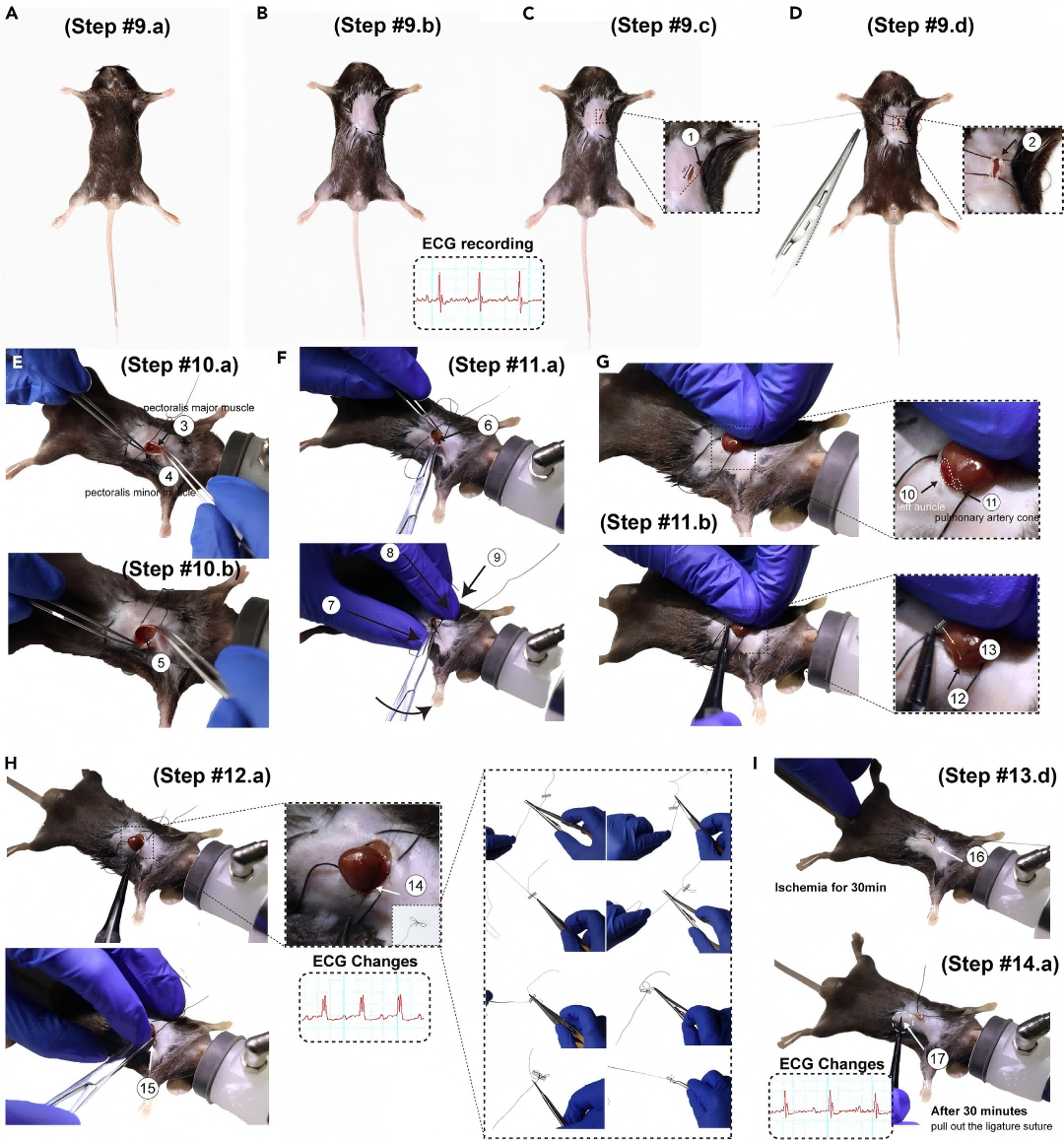
图3. 心肌缺血再灌注模型制备的详细流程图
达到预设缺血时间后,松解活结/滑结,恢复冠脉灌注。
再灌注判定:ECG中ST段回落至基线作为再通恢复的证据;建议记录解除阻断前后心电变化用于质控留档。
回纳心脏后进行胸腔排气:可用双手拇指与食指轻轻挤压胸廓1–2次以减少气体残留,随后尽快缝合胸壁与皮肤。
术后复苏:置于约30°C恢复环境,持续观察呼吸、活动与疼痛表现直至清醒。
镇痛:美洛昔康1–2mg/kg皮下注射,持续2–3天。
抗感染:头孢噻呋钠5mg/kg,必要时连续2–3天。
每日观察:体重、活动度、呼吸情况与切口状况,异常及时处理并记录。
按预设再灌注窗口处死取心。
组织学:心脏固定、石蜡包埋与切片,进行HE及Masson染色,并可用ImageJ进行面积/结构定量。
功能学:心脏超声评估左室内径与射血分数等指标,用于重构与心功能随访。
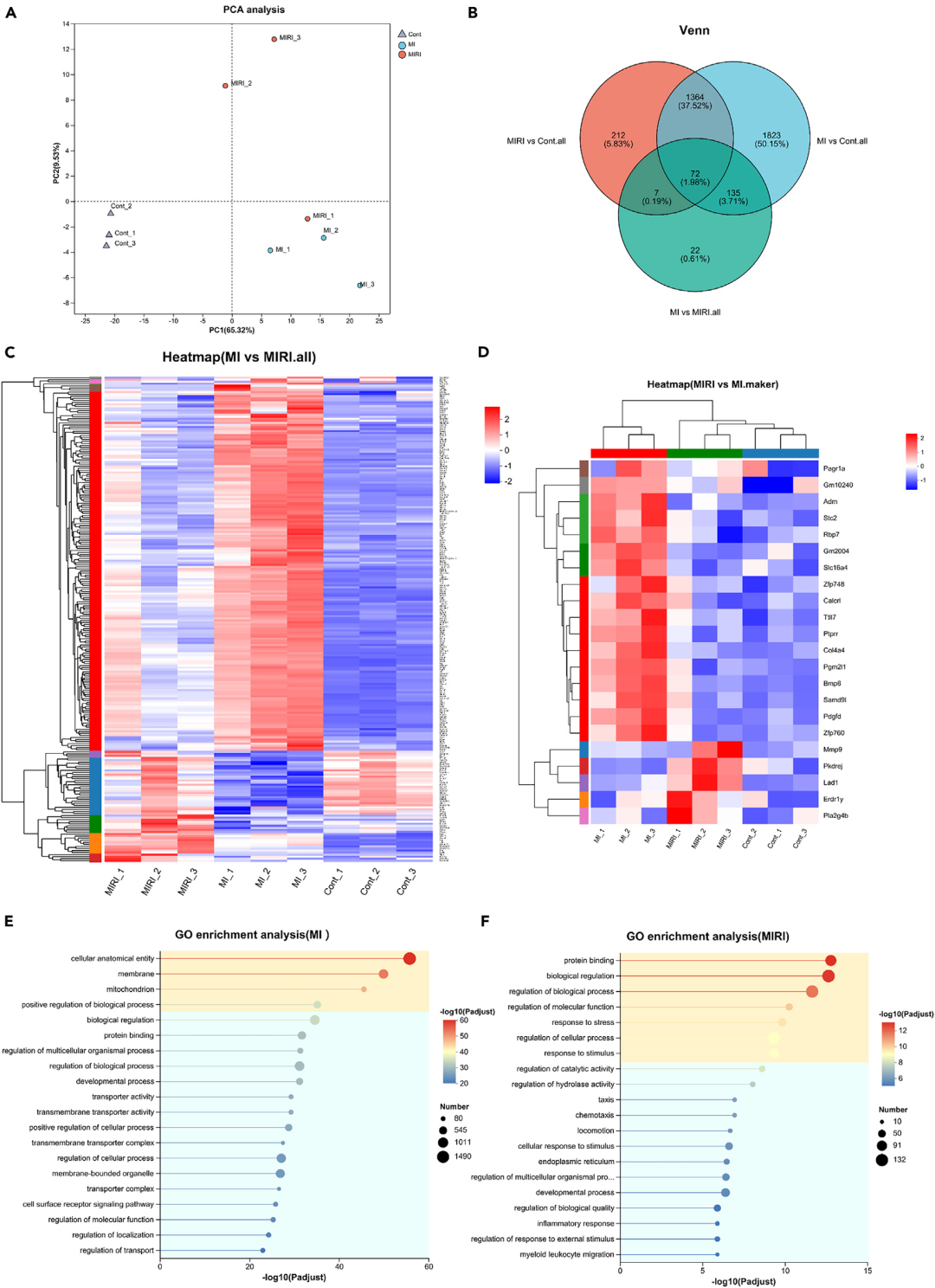
图4. RNA测序分析揭示MI与MIRI的基因表达特异性
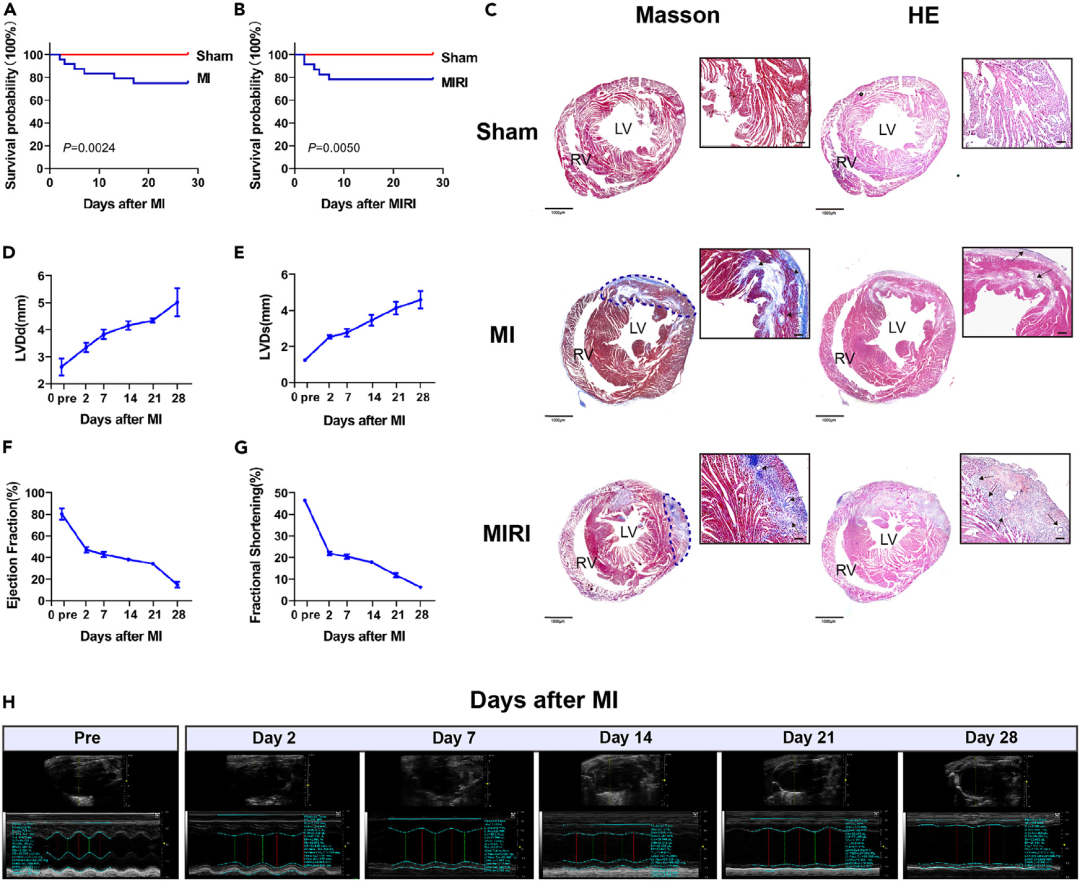
图5. LAD结扎后的超声心动图与组织学分析
缺血需要有明确判定依据:建议同时记录心肌前壁颜色变浅/发白等肉眼变化,并保留ECG缺血表现(如ST段抬高)。
再灌注需要有明确判定依据:解除阻断后,ST段回落至接近基线可作为再灌注恢复的重要证据,建议保存解除前后对应的心电记录片段。
结扎位置必须保持一致:结扎点高低偏差会改变危险区范围,从而影响梗死面积与炎症指标的横向可比性。
气胸:闭胸前务必排气并尽快缝合,操作器械尽量钝性以减少肺损伤风险。
心律失常:多与LAD定位不准、结扎过高/过宽/过深相关,需优化定位与结扎深度。
麻醉过量:诱导时间过长或维持浓度过高可致呼吸抑制,需持续监测呼吸并及时调整。
出血与心肌撕裂:穿刺或拉线用力过大可撕裂心肌;解除结扎线时动作应小且缓慢,避免心肌破裂出血。
建议为每只动物建立最小记录包:诱导/维持麻醉参数、呼吸频率与体温、缺血与再灌注心电证据、术后镇痛抗感染给药记录、死亡或剔除原因。
同批次实验尽量统一缺血时长、再灌注窗口、结扎高度与术后管理方案,减少批间漂移。