CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化

实验结果一:在活体里直接看到氯胺酮诱导的腺苷动态上升
作者首先用遗传编码腺苷探针GRABAdo1.0结合多通道光纤记录,在小鼠脑内实时追踪细胞外腺苷变化,并用失活突变体与急性低氧刺激完成信号有效性校验。在此基础上,系统给药氯胺酮后,内侧前额叶皮层与海马出现快速且持续的细胞外腺苷升高,而伏隔核变化不明显,提示该效应具有脑区特异性。该结果把腺苷从“候选相关因子”推进为“可量化的动态表型”,为后续因果验证提供入口。
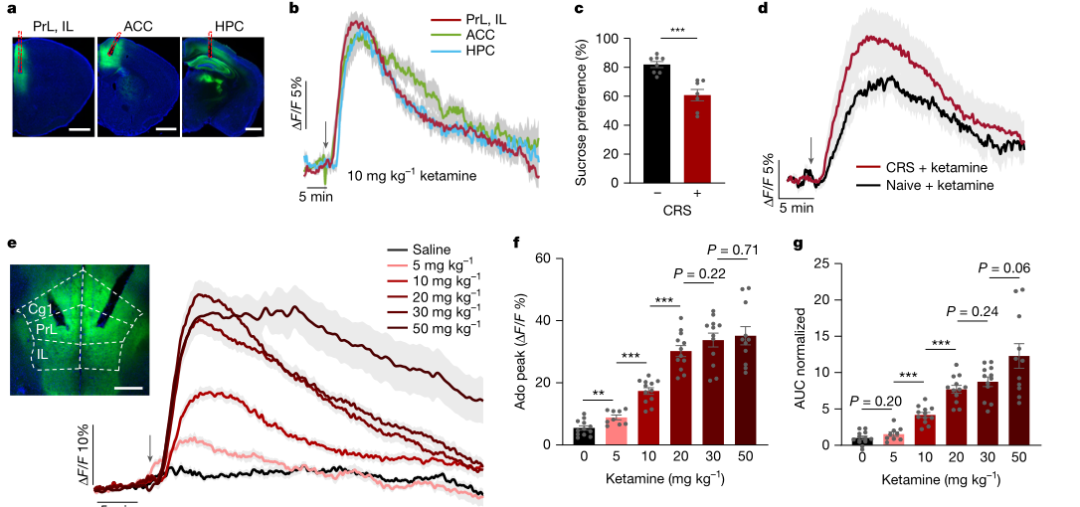
图1 氯胺酮在脑内诱发腺苷瞬时升高
实验结果二:腺苷信号驱动氯胺酮的抗抑郁效应且A1/A2A受体是必需环节
在慢性束缚应激等抑郁模型中,氯胺酮能够快速改善绝望样与快感缺失相关行为;但当A1受体或A2A受体被遗传缺失,或用受体拮抗剂进行药理阻断时,上述行为学获益显著削弱甚至消失,覆盖急性与持续两个时间维度。这一组结果将“腺苷上升”与“抗抑郁效应”从相关性推到受体层面的必要性。进一步地,外源给予腺苷或选择性激动A1与A2A受体可在短时间内复制抗抑郁样效应,提示该通路不仅必需,且在一定条件下具有致效充分性。
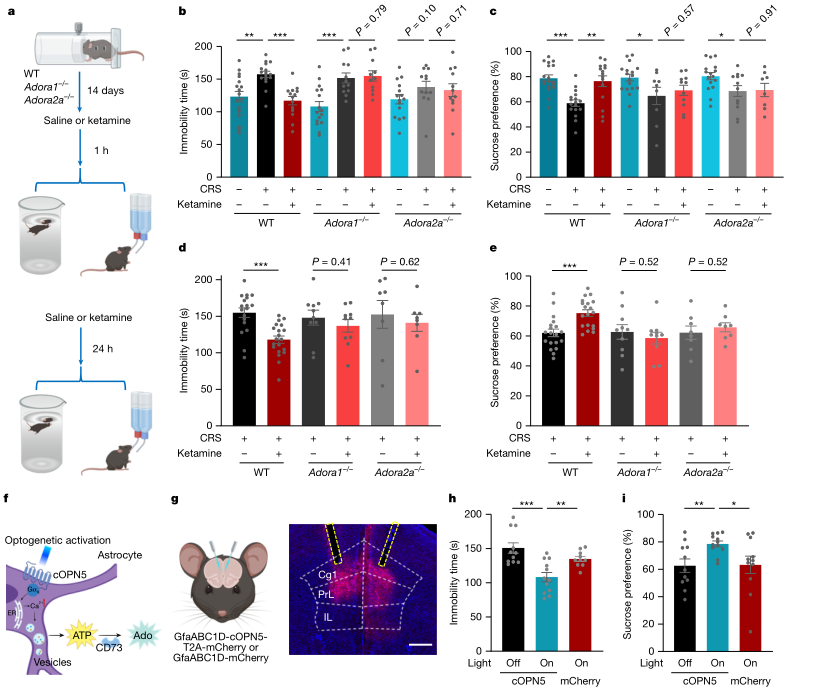
图2 腺苷信号驱动氯胺酮的抗抑郁作用
实验结果三:关键空间节点定位于mPFC并由局部受体表达决定疗效能否发生
为避免机制泛化,作者将因果进一步定位到内侧前额叶皮层。mPFC局部给予腺苷可以产生显著的抗抑郁样效应;而在成年动物mPFC内通过AAV递送CRISPR-Cas9体系局部敲低A1或A2A受体后,系统给药氯胺酮的行为学疗效被消除。相对地,将相似策略转移到其他脑区并不能稳定复现同等行为学获益,说明mPFC腺苷受体通路是该快速效应链条中的关键空间环节。
实验结果四:腺苷来自代谢驱动的细胞内生成并经ENT1/2外排而非依赖细胞外核苷酸水解
作者针对“腺苷从何而来”给出分层排除与正向证据。实时监测显示氯胺酮并不引起细胞外ATP/ADP显著上升,且CD73相关途径并非该场景的主导来源,支持“细胞外核苷酸水解生成腺苷”不是核心路径。相反,抑制ENT1/2可明显削弱氯胺酮诱导的细胞外腺苷上升,提示腺苷主要在细胞内累积后通过转运体外排。进一步的能量状态读数与线粒体代谢通量实验显示,氯胺酮在治疗相关浓度下可重塑线粒体代谢、影响能量平衡,为“ATP/ADP变化→细胞内腺苷增加→ENT介导外排→受体激活→行为学改善”提供上游机制支撑。同时,Ca²⁺活动监测未见有效剂量下mPFC锥体神经元出现显著过度兴奋式增强,提示该链条更符合代谢驱动的腺苷调节模式。
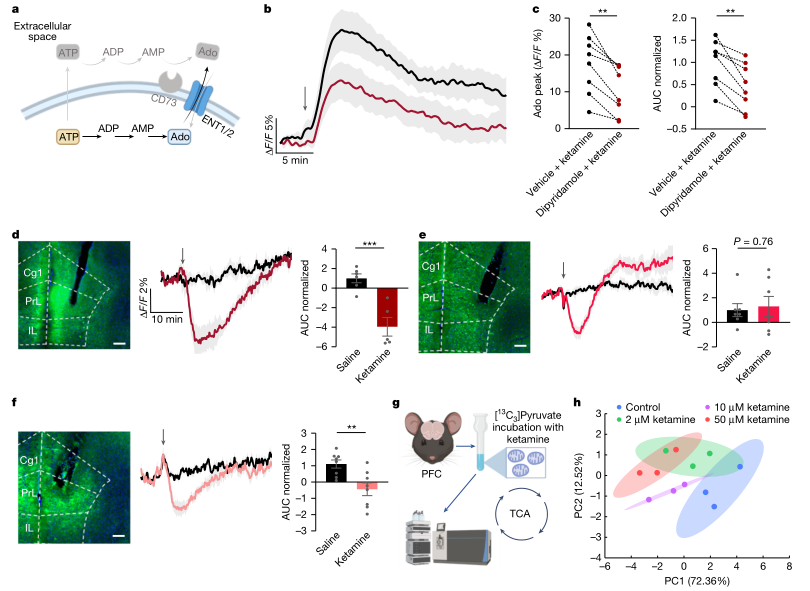
图3 氯胺酮重塑细胞代谢并通过ENT1/2促进腺苷外排
实验结果五:把机制变成研发工具,用腺苷动力学筛选并验证更优类似物
作者将mPFC腺苷动态作为功能性生物标志物,构建表型驱动的化合物筛选流程,对多种氯胺酮衍生物进行合成与体内读数比较。结果显示,部分候选可诱导更强或更持久的腺苷上升,并在抑郁模型中以更低剂量实现与氯胺酮相当的行为学改善,同时在运动相关副反应上更轻。该策略的关键价值在于,用“疗效相关的动态信号”替代单一受体亲和力或终点行为学作为优先筛选轴,使分子优化更可解释、也更可迭代。
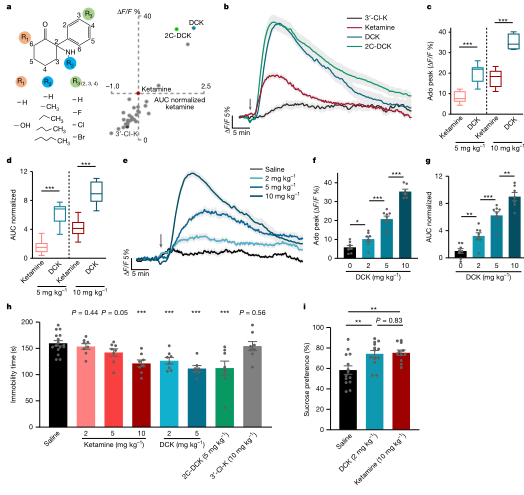
图4 基于腺苷信号的筛选发现具有强抗抑郁样效应的氯胺酮类似物
实验结果六:腺苷通路同样解释ECT的快速抗抑郁效应并提供跨干预的统一机制
作者将同一套腺苷实时记录与受体依赖性验证拓展到电休克治疗相关范式。ECT诱发的发作过程中,mPFC细胞外腺苷出现显著上升;在抑郁模型中,ECT的行为学获益同样依赖A1与A2A受体,提示腺苷信号是药物与物理干预共享的关键节点。这一结果强化了腺苷机制链条的外推性,并为后续组合疗法或替代性快速干预提供共同的可操作靶点。
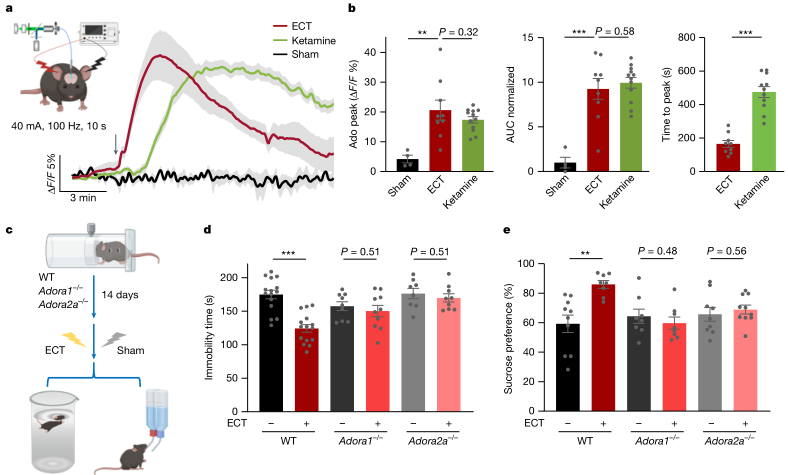
图5 腺苷信号对电休克治疗的抗抑郁效应至关重要
实验结果七:可控低氧训练可通过同一腺苷节点产生抗抑郁样效应
作者进一步引入急性间歇低氧训练方案,通过低氧与常氧交替循环在mPFC诱导腺苷上升并改善抑郁相关行为;当A1或A2A受体缺失时,该改善不再出现,说明该非药物干预同样汇聚到腺苷受体通路。这为围绕腺苷节点的“可控、可重复、可分层”的干预策略打开空间。
扩展数据
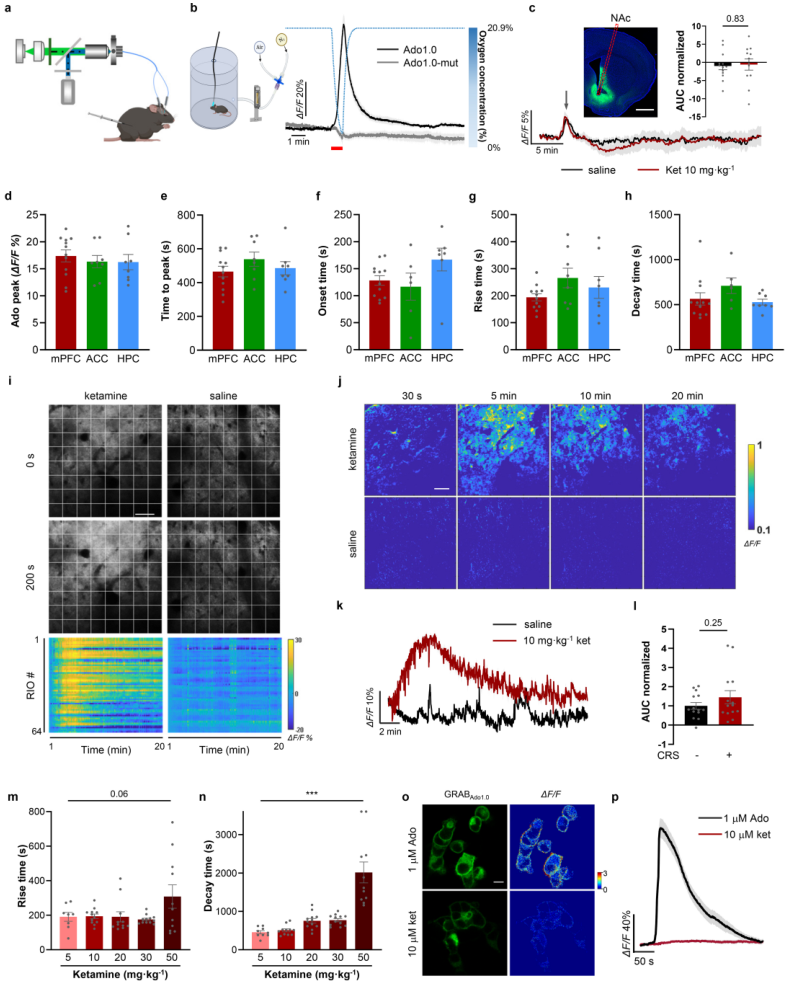
扩展数据图1|氯胺酮诱导腺苷信号的表征与验证
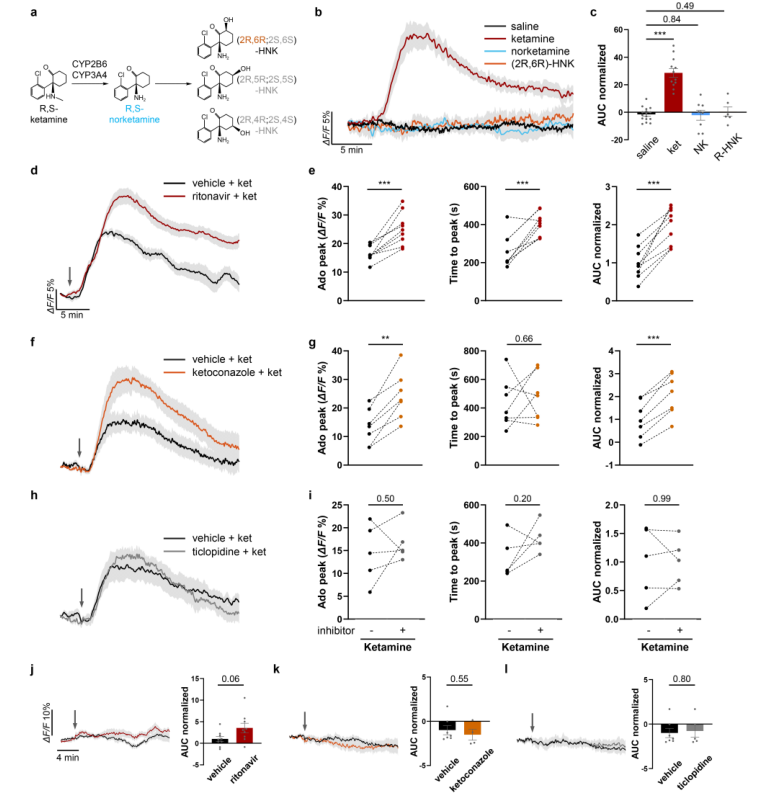
扩展数据图2|氯胺酮代谢物与代谢抑制剂对mPFC腺苷释放的影响
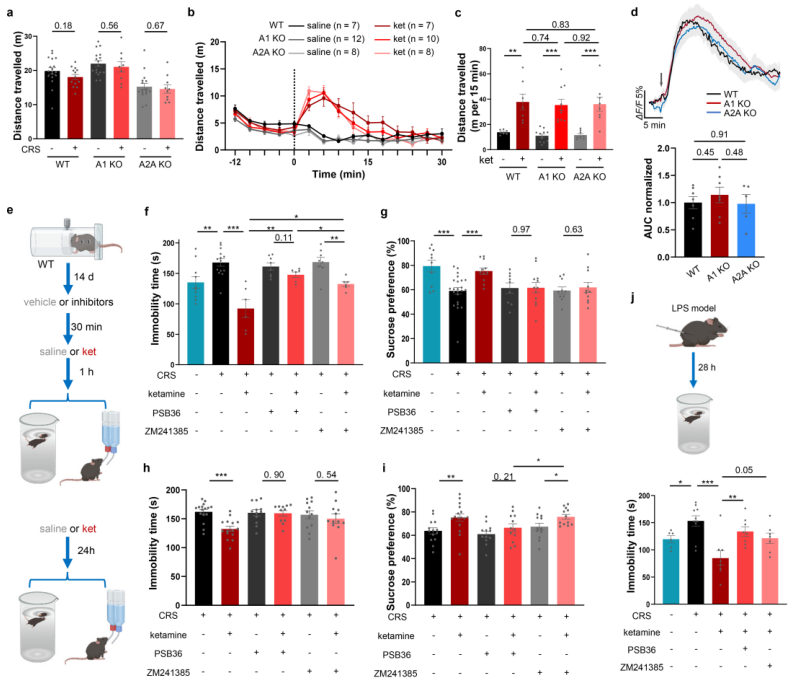
扩展数据图3|腺苷受体活性对氯胺酮抗抑郁效应至关重要,且不改变运动活动与腺苷释放
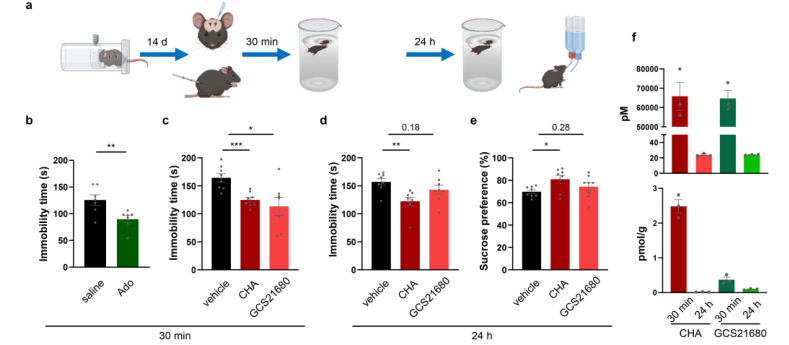
扩展数据图4|激活腺苷受体可产生抗抑郁样效应
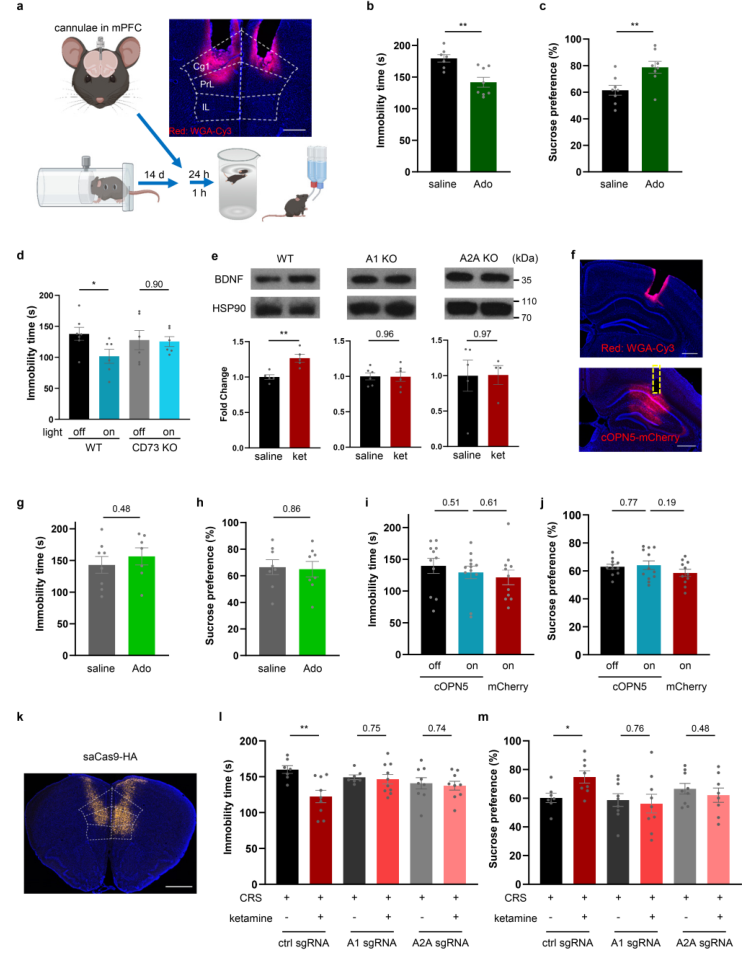
扩展数据图5|腺苷介导效应的脑区特异性
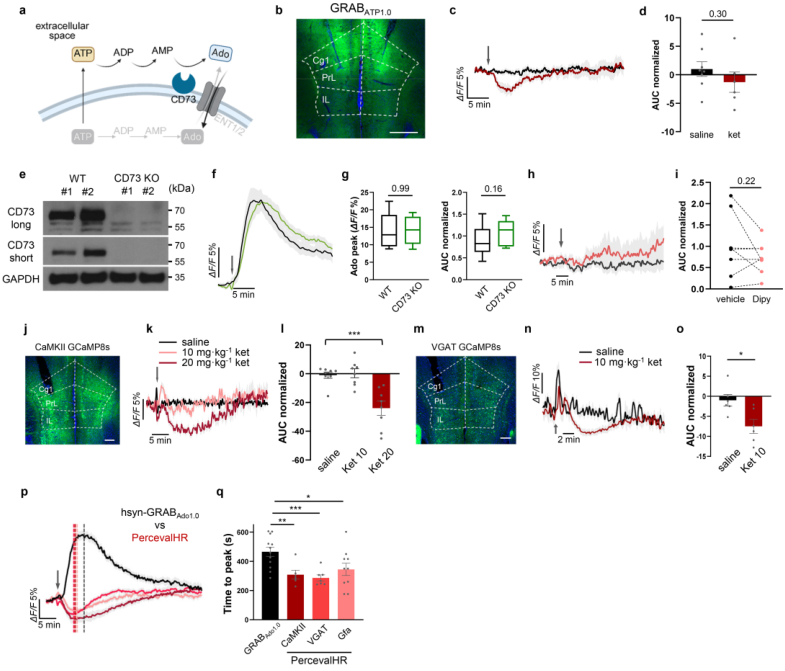
扩展数据图6|氯胺酮诱导的腺苷瞬时升高不依赖细胞外ATP水解,也不依赖广泛神经元过度激活
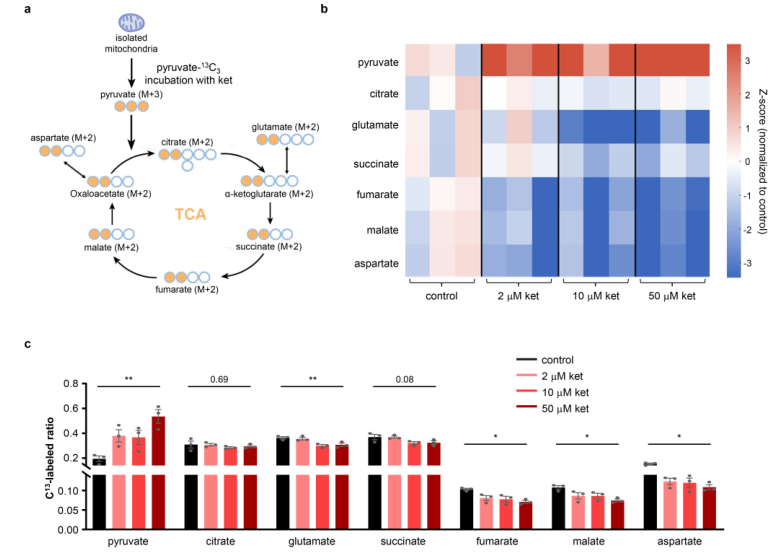
扩展数据图7|氯胺酮直接调控线粒体TCA循环通量
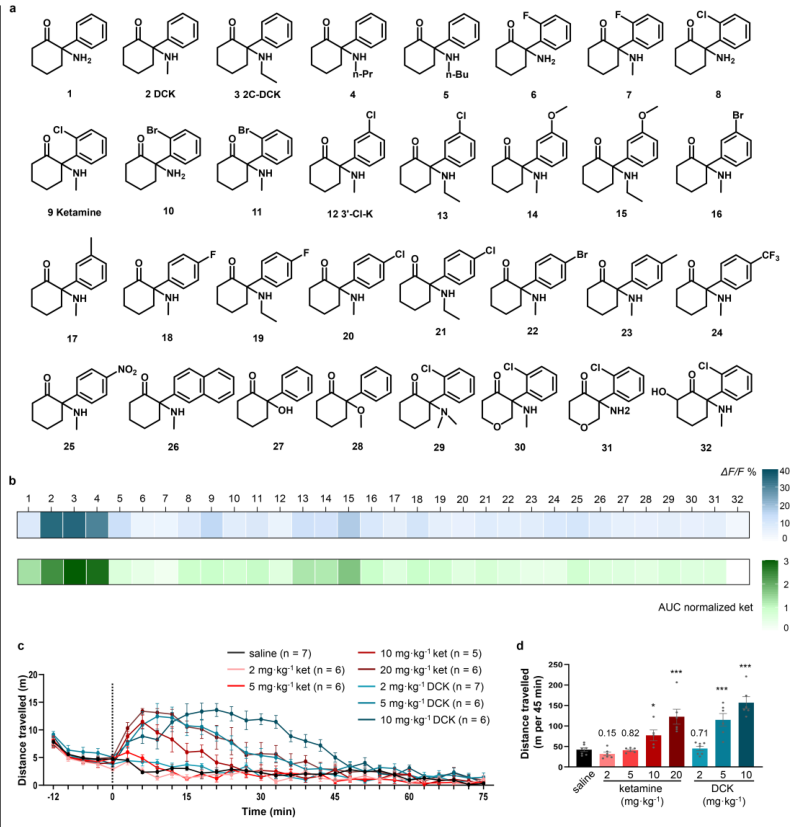
扩展数据图8|氯胺酮类似物的体内表征:腺苷释放与运动活动
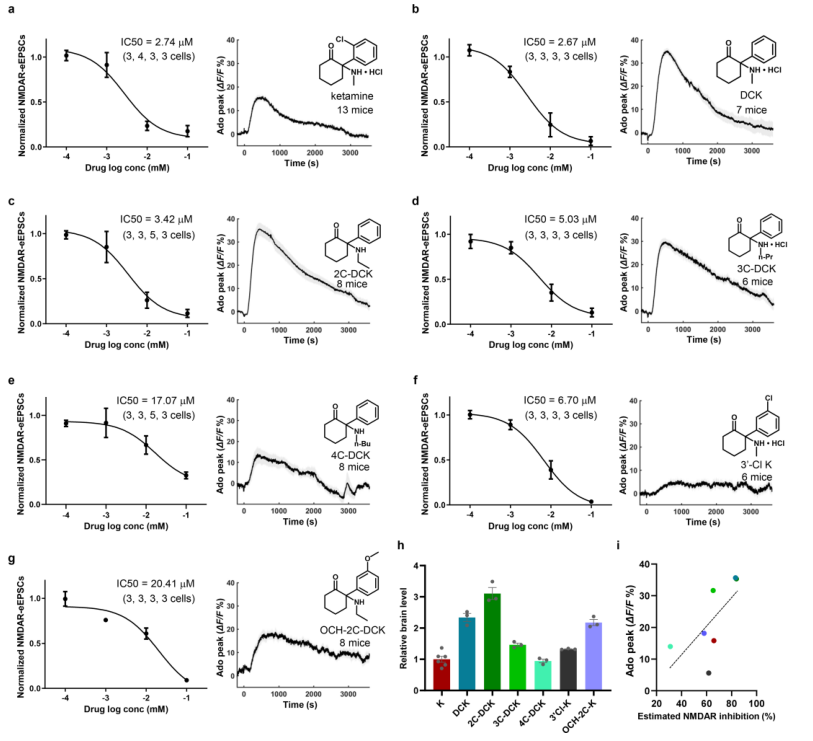
扩展数据图9|氯胺酮类似物对NMDA受体阻断与腺苷调节的比较分析
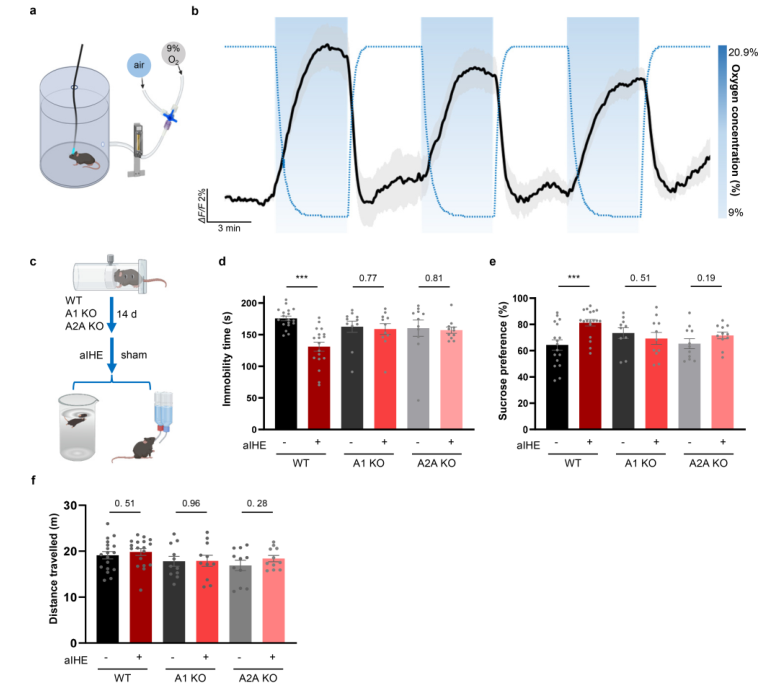
扩展数据图10|急性间歇低氧(aIH)通过腺苷信号缓解抑郁样表型
结语
本文的核心贡献在于以动态测量为起点,连续完成受体因果验证、脑区定位、上游代谢来源解析与转化筛药闭环,使腺苷从相关指标升级为可操作的机制枢纽。后续研究若要继续推进,重点应放在mPFC腺苷信号的时间窗、细胞类型贡献与副作用解耦机制上,并沿用同一套动态读数体系来比较不同快速干预的共性与差异,从而形成更可控的治疗设计路径。
参考文献:Yue C, Wang N, Zhai H, Yuan Z, Cui Y, Quan J, Zhou Y, Fan X, Wang H, Wu Z, Mi H, Ge W, Li Y, Wang X, Luo M. Adenosine signalling drives antidepressant actions of ketamine and ECT. Nature. 2026 Jan;649(8096):423-431. doi: 10.1038/s41586-025-09755-9. Epub 2025 Nov 5. PMID: 41193806; PMCID: PMC12779573.