CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
发表在《Science》上的这项研究指出,急性肾损伤并不只是一次短暂打击,它会在肾小管细胞内留下持续存在的线粒体DNA异质性突变,降低肾脏面对下一次损伤时的韧性。研究还提示,这种长期脆弱状态与嘌呤代谢受抑以及腺苷-AK4轴功能下降有关。
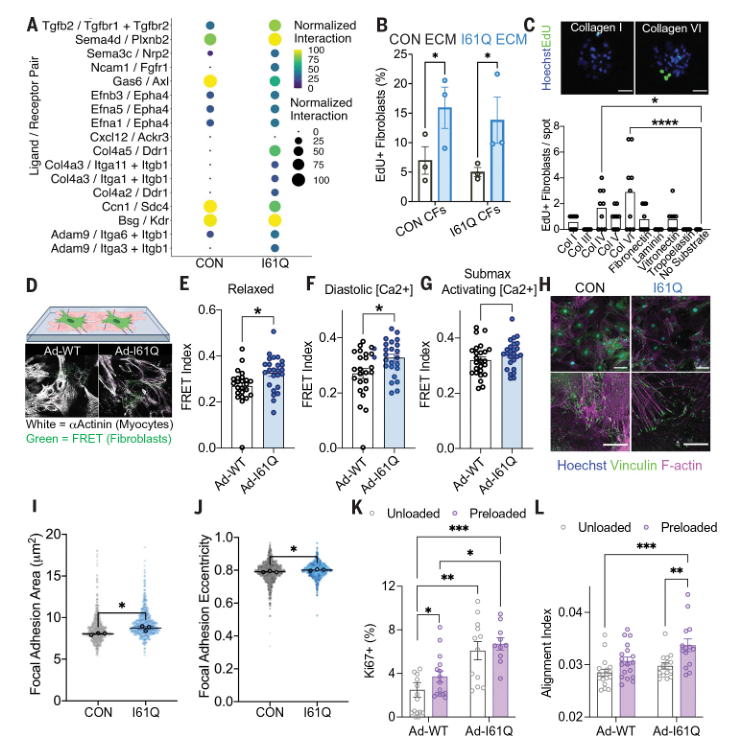
图1 细胞外基质-受体相互作用增强成纤维细胞的舒张期机械感知,并驱动其增殖。
AKI向CKD进展一直是肾脏医学中的难点。很多患者在急性期后肌酐可以回落,但之后仍会出现肾功能持续下降、纤维化加重以及再损伤风险升高。既往解释多集中在炎症、氧化应激和微循环障碍。这项研究进一步提出,急性损伤还会把“分子记忆”留在线粒体基因组层面,成为后续代谢脆弱性的基础。
作者在缺血再灌注和叶酸诱导两类AKI模型中都观察到类似现象:肾组织内携带替代等位基因的mtDNA位点在急性期明显增加,而且这种增加会持续到慢性阶段。更关键的是,突变负担越高,急性损伤越重,后期纤维化也越明显。体外实验同样显示,氧化应激可引起肾小管细胞mtDNA损伤增加,并伴随ATP生成下降。
机制上,问题集中在能量代谢。mtDNA突变负担升高后,细胞线粒体呼吸下降,虽然糖酵解有所代偿,但总体ATP仍然不足。代谢组结果显示,受影响最明显的是嘌呤代谢,尤其是腺苷、AMP和ADP等分子水平下降。在多种核苷中,真正能够明显恢复ATP生成、改善线粒体功能并减轻纤维化标志物升高的,主要是腺苷。进一步分析提示,AK4下调会削弱这种保护作用,说明腺苷进入代谢网络后,需要依赖AK4相关过程来支持ATP再生。
这项工作的价值还在于临床关联。患者肾组织分析显示,mtDNA替代等位基因丰度与eGFR相关,且eGFR低于60mL/min/1.73m²的人群突变负担更高。UKBiobank纳入369,912名参与者,其中18,012人发生新发AKI。按mMSS计算,每增加1个标准差,eGFR平均下降0.71mL/min/1.73m²,未来AKI风险增加1.25倍;校正eGFR后,这种关联仍然存在。这说明mtDNA突变负担并不只是伴随现象,而可能直接参与决定肾脏后续结局。
从概念上看,这项研究把AKI后的“恢复”重新定义了。肾脏是否真正恢复,不能只看常规功能指标是否回落,还要看线粒体基因组和能量代谢系统是否恢复到可承压状态。治疗上,mtDNA异质性负担可能成为风险分层指标,围绕腺苷补充、嘌呤代谢支持或AK4相关通路的干预也值得继续推进。不过,这些策略目前仍主要停留在机制验证阶段,距离临床应用还需要更多关于剂量、安全性和适用人群的研究。
这项研究把AKI后持续存在的mtDNA异质性突变从背景推到前台,并提示修复腺苷-AK4轴、改善ATP再生能力,可能成为延缓AKI向CKD进展和降低再损伤风险的一个新切入口。