CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
动脉粥样硬化是心脑血管疾病研究中的核心病理基础,其发生发展与脂质代谢异常、血管内皮损伤、炎症细胞浸润、泡沫细胞形成和斑块稳定性变化密切相关。在实验研究中,ApoE基因缺陷小鼠因成模稳定、遗传背景清楚、斑块特征接近人类病变,成为动脉粥样硬化模型中使用较多的一类基因工程动物模型。
ApoE即载脂蛋白E,是脂蛋白代谢过程中的关键调控因子。ApoE基因缺陷后,小鼠脂质转运和清除能力下降,容易出现血脂水平升高,并逐渐形成高脂血症和动脉粥样硬化病变。与单纯依靠高脂饲料诱导的模型相比,ApoE基因缺陷小鼠具有更明确的遗传基础,病变形成路径更清晰,适合用于疾病机制研究和药物干预评价。
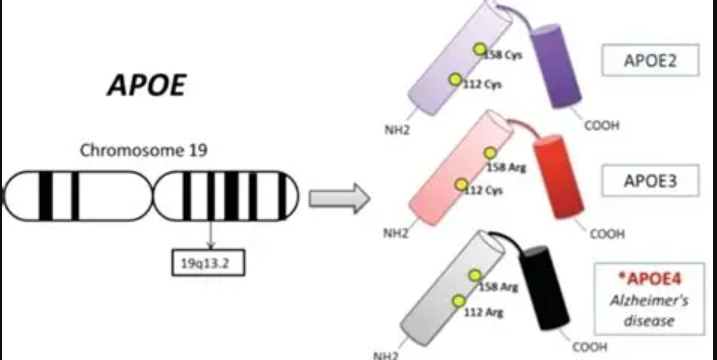
ApoE载脂蛋白
在常见建模方案中,6~8周龄ApoE基因缺陷小鼠可采用西方类型膳食饲喂。该类饲料通常具有较高脂肪和胆固醇含量,可促进血脂升高和血管斑块形成。经过一定周期饲喂后,小鼠主动脉根部、主动脉窦、冠状动脉等部位可出现明显的动脉粥样硬化斑块。病理表现包括血管内膜增厚、泡沫细胞聚集、脂质核心形成、纤维帽出现以及局部炎症细胞浸润。
随着饲喂时间延长,模型病变会进一步加重。HE染色下可观察到主动脉根部明显斑块结构,部分病灶可出现纤维帽变薄、脂质核心扩大、巨噬细胞聚集、血管中膜结构破坏、钙化和萎缩等表现。这些变化与人类动脉粥样硬化斑块从早期脂质条纹向成熟斑块发展的过程具有一定相似性,因此ApoE基因缺陷小鼠常用于AS斑块进展、斑块稳定性和易损斑块相关研究。
该模型的一个突出特点是血脂水平与人类高脂血症状态较为接近。资料显示,ApoE基因缺陷小鼠成模后血总胆固醇水平可达到3~5g/L,相比部分高脂高胆固醇饲料诱导模型中总胆固醇异常升至7~10g/L的情况,更利于模拟相对接近临床病理背景的脂质代谢异常状态。对于研究降脂药物、抗炎干预、抗氧化治疗、斑块稳定化策略等方向,该模型具有较高参考价值。
从实验应用角度看,ApoE基因缺陷小鼠具备个体小、用药量少、繁殖能力较强、饲养和操作相对便利等优势。其病变部位明确,主动脉根部和主动脉窦常作为组织学观察重点,可结合HE染色、油红O染色、免疫组化、血脂检测、炎症因子检测和分子生物学分析,对模型表型和干预效果进行系统评价。
在药效学研究中,该模型可用于抗动脉粥样硬化药物、降脂药物、抗炎药物、天然产物活性成分及新型递送系统的体内验证。通过比较不同干预组小鼠血脂水平、斑块面积、泡沫细胞数量、巨噬细胞浸润程度、胶原含量和纤维帽厚度,可以较直观地反映药物对AS发生发展的影响。
总体来看,ApoE基因缺陷小鼠动脉粥样硬化模型兼具遗传背景明确、成模表现稳定、病理特征典型和应用场景广泛等特点。对于高脂血症、血管炎症、泡沫细胞形成、AS斑块进展及抗动脉粥样硬化药物筛选研究,该模型仍是较为成熟且具有代表性的实验动物模型。