CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化

这篇发表于《Cell》的综述给出的核心判断是:RNA修饰,尤其是m6A,已经不能再被视为转录后层面的背景标记,而是在染色质调控、转录程序、肿瘤代谢和免疫微环境重塑中都具有实质性的调控地位,并且这些基础认识已经开始进入治疗开发阶段。它值得关注,不只是因为RNA修饰的分子图谱仍在快速扩展,更因为这一层调控能够把抗原递呈、糖酵解、乳酸积累和免疫检查点应答放进同一条机制链条里,为肿瘤治疗提供一个比单纯基因突变解释更动态的分析框架。
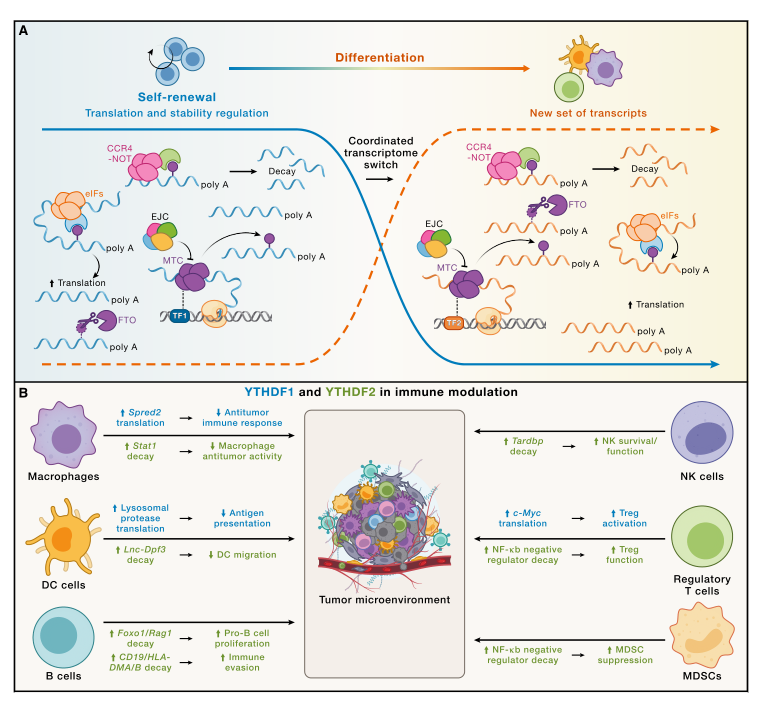
mRNA的m6A在肿瘤微环境中调控细胞自我更新、分化与免疫应答的作用
肿瘤进展,尤其是转移和免疫治疗失败的解释,过去更多依赖DNA突变、经典表观遗传和蛋白信号通路三个层面。但这篇综述提示,RNA修饰本身就是决定基因表达时序、细胞状态切换和治疗反应差异的重要变量。目前已鉴定出超过170种RNA化学修饰,其中m6A是内部mRNA中最丰富的一类。作者总结,单条mRNA通常可见约2–3个m6A位点,而内部m6A总体丰度约为capm6Am的10–30倍。这意味着RNA修饰既足够广泛,也具备足够的调控强度,能够深入影响肿瘤相关通路,而不是只产生边缘性的表达波动。
在肿瘤免疫微环境中,综述梳理出的第一条代表性主线,是m6A读取蛋白如何改变抗原信息从树突状细胞传递到CD8+T细胞的效率。YTHDF1在肿瘤细胞和免疫细胞中都可上调,其中在树突状细胞内,YTHDF1相关程序会压低抗原交叉递呈效率,结果不是抽象的免疫抑制,而是更具体的CD8+T细胞启动不足和抗PD-L1疗效下降。这里并不是某种代谢物在供受体细胞之间直接转运,而是树突状细胞对肿瘤来源抗原的处理程序被RNA修饰读取机制重写,最终把影响传递给效应T细胞。也正因此,RNA修饰开始从细胞内分子调控问题,转成可以改变免疫治疗结果的微环境变量。
另一条机制主线把RNA修饰与肿瘤代谢和免疫抑制生态位连在了一起。综述指出,FTO的遗传敲低或药理抑制可削弱肿瘤细胞糖酵解,恢复CD8+T细胞功能并抑制肿瘤生长;ALKBH5则可通过调节乳酸相关通路,促进抑制性免疫细胞积累,从而压低抗PD-1应答。与此同时,在肿瘤相关巨噬细胞中,METTL3-METTL14介导的m6A可推动Spred2和Stat1翻译,改变TAM状态,并提高对抗PD-1治疗的敏感性。也就是说,RNA修饰通过糖酵解、乳酸和翻译程序把多类细胞绑进同一张代谢—免疫网络。
从临床相关性看,这篇综述明确提到,YTHDF1在肿瘤组织及癌旁组织中的水平与CD8+T细胞浸润和免疫检查点抑制剂疗效呈负相关,说明RNA修饰读者蛋白并不只是细胞实验现象,而是已经能够在患者组织层面映射到免疫状态差异。因果证据则更多来自功能干预:FTO敲低或药理抑制可降低肿瘤糖酵解并恢复CD8+T细胞功能,ALKBH5和TAM内METTL3-METTL14通路的干预也会改变抗PD-1应答。需要指出的是,这是一篇综述而非单一原始研究,作者并没有像机制论文那样统一报告患者队列样本量、HR值或ROC值,因此临床证据更接近方向性归纳,而不是单队列闭环验证。
这篇文章推动我们重新理解免疫—肿瘤互作和肿瘤代谢来源。过去常把免疫抑制理解为细胞组成变化,把代谢重编程理解为肿瘤细胞的内生性质;而这里的图景是,RNA修饰把转录本命运、翻译效率、糖酵解、乳酸堆积、抗原递呈和免疫检查点疗效串成了连续过程。对应到治疗层面,潜在策略也因此不止一种:既可以考虑直接靶向FTO、ALKBH5、METTL3等读写擦因子,也可以把RNA修饰状态作为分层标志物,与抗PD-1/PD-L1治疗联用。作者同时指出,这一方向已从基础研究走向治疗开发,已有候选策略进入临床试验阶段,但真正可用的药物窗口、肿瘤类型选择和细胞类型特异性,仍需要进一步验证。
RNA修饰已经从基因表达调控的背景层,前移为决定肿瘤代谢、免疫逃逸和治疗反应的重要前台变量,而以m6A读写擦网络为切入口的联合干预,正在成为值得认真评估的新方向。
DOI:10.1016/j.cell.2026.01.006