CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
《Science》这篇研究的核心结论是,老年肌肉干细胞再生变慢,并不只是因为“老化后功能普遍变差”,还与NDRG1上调后形成的一种细胞生存偏差有关。它一方面压低mTOR相关活化程序,提升细胞在长期中的存活潜力,另一方面也让肌肉干细胞更难迅速退出静息、进入增殖与修复过程。这个发现值得重视,因为它把老年肌肉再生迟缓的问题,从“功能衰退”推进到“细胞群体在衰老过程中被重新筛选”,也提示某些衰老相关改变未必只是负担,本身也可能带有维持细胞池的代偿意义。
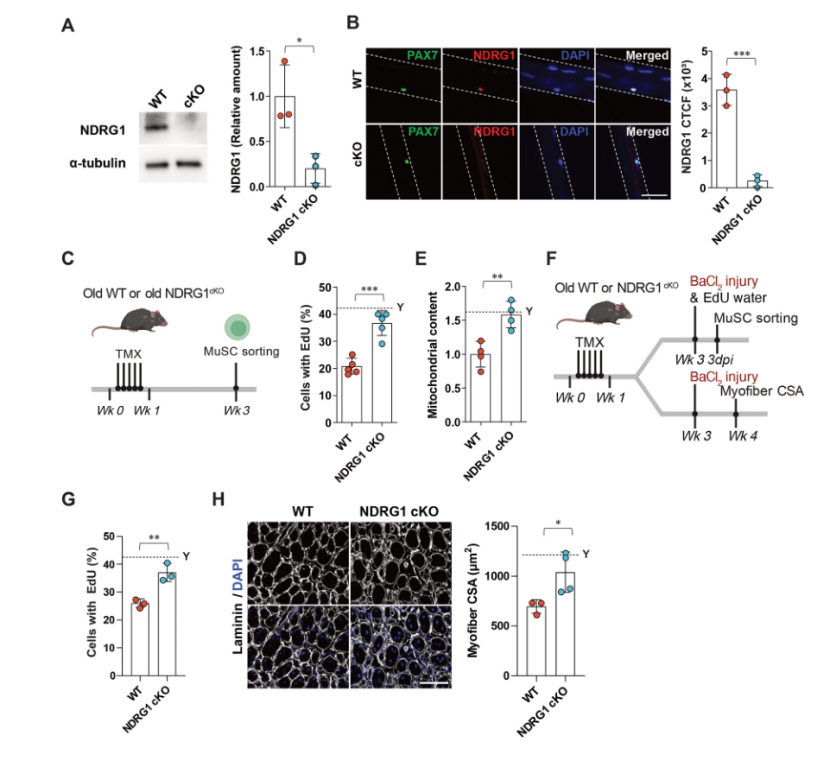
在老年MuSC中敲除NDRG1后,MuSC活化增强且肌肉再生改善
骨骼肌老化最直观的后果之一,是损伤后修复速度下降,而肌肉干细胞从静息态转入活化和细胞周期的过程明显延迟,被认为是这一现象的关键基础。过去的主流解释多集中在DNA损伤累积、表观遗传漂移、干性下降以及生态位老化等方向,重点放在老年细胞本身越来越难以胜任修复任务。老年组织里留下来的,未必是最适合再生的那批肌肉干细胞,而更可能是更耐受、更能存活、但启动更慢的细胞。这样一来,老年肌再生迟缓不只是单细胞能力下降的问题,也可能是整个细胞群体组成在长期压力下发生了方向性偏移。
研究者首先从年轻和老年小鼠的肌肉干细胞转录组入手,发现两者已经出现明显分群。在差异基因中,NDRG1是非常突出的一个信号,它在老年肌肉干细胞中显著上调,RNA水平约增加3.5倍,随后又通过免疫荧光和蛋白检测得到确认。
这里最关键的一点是,文章讨论的并不是某种细胞间货物转运过程,也不是经典意义上的“谁给谁递送代谢底物”,而是同一种肌肉干细胞在衰老进程中被逐渐筛选出不同状态。也就是说,老年肌肉里富集的是高NDRG1状态的肌肉干细胞,它们更倾向于保留自身生存能力,却不擅长快速响应损伤刺激。
进一步的机制分析显示,NDRG1主要是在肌肉干细胞内部充当制动器,抑制PI3K-AKT-mTOR信号轴。研究者结合转录组富集分析、p-mTOR和p-AKT检测、EdU掺入实验、线粒体积累分析以及流式细胞术,证明老年肌肉干细胞一旦失去NDRG1,就更容易进入S期,线粒体含量增加,细胞体积增大,并呈现出更接近GAlert样的预激活状态。
NDRG1高表达使老年肌肉干细胞维持在一种更保守、更克制的状态,避免过早消耗;而当这一制动解除后,细胞会更快投入修复,但也更容易在持续应激中付出代价。雷帕霉素能够部分逆转这种变化,说明NDRG1对肌肉干细胞命运的调节,核心确实在于mTOR这一枢纽。
NDRG1缺失后,老年肌肉干细胞的EdU阳性比例明显上升,大致可从约20%提高到约36%至40%,说明其进入增殖程序的能力增强;与此同时,细胞激活阶段的死亡率也从约20%升至约40%,提示这种“提速”不是无代价的。
更关键的是,在第一次损伤修复中,缺失NDRG1的老年肌肉干细胞确实表现出更快的再生反应,但在重复损伤模型里,其再生质量反而下降,中央核肌纤维横截面积大致由约1700μm²降至约1200μm²。这组结果非常关键,因为它说明NDRG1并不是简单地“妨碍修复”,而是在短期再生效率和长期细胞池维持之间,帮助老年肌肉干细胞做了一种偏向生存的取舍。
这项研究的概念意义很强,因为它迫使我们重新理解干细胞衰老。很多时候,组织功能下降并不只来自“每个细胞都变差了”,还可能来自“最后活下来的细胞类型变了”。老年肌肉干细胞群体之所以修复迟缓,未必只是因为细胞普遍衰老,也可能是因为长期筛选留下了更擅长自保、却不擅长快速修复的一群细胞。沿着这个思路,未来的治疗策略可能不该简单粗暴地持续激活肌肉干细胞,而更可能需要时序化干预,例如在急性损伤早期短暂解除NDRG1-mTOR的制动,提高修复启动速度,随后再恢复保护机制,以免过度消耗干细胞池。