CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
01肠–免疫–骨轴的整体视角
说到骨质疏松,很多人的第一反应还是钙片、维生素D、双膦酸盐这些经典组合。不过这几年不管是文章选题还是项目立项,话题慢慢聚焦到“肠道菌群”“免疫老化”“慢性炎症”这一整条链。这篇发在 Journal of Advanced Research 的工作,把一个早就用在婴幼儿配方里的分子——2'-岩藻糖基乳糖(2'-FL,人乳寡糖代表成分之一)拉进了老年骨质疏松赛道。作者没有紧盯骨骼单一靶点,而是顺着“肠–免疫–骨”这条当下最热门的通路,从肠道屏障和微生态入手,接着抓免疫极化,最后落到骨重塑。
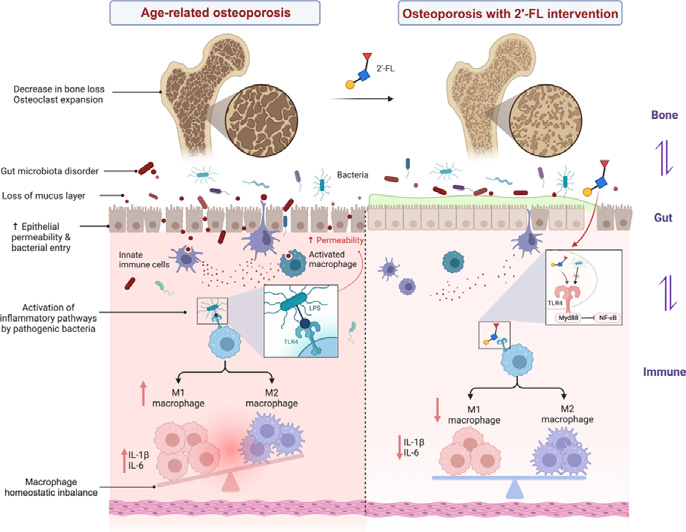
02自然老龄骨质疏松模型的关键证据
这篇文章模型选取自然老龄小鼠,而不是常规的卵巢切除或药物诱导。对标的是更贴近真实人群的那种“免疫老化+微生态失衡+骨量持续下滑”的复合状态。micro-CT 三维重建配合 H&E、TRAP 等染色,画面非常直观:老年组股骨松质骨小梁变稀、变细、断裂多,空洞明显增多;持续口服 2'-FL 12 周后,小梁重新变得致密、连续,BV/TV、Tb.N 这些指标往上走,Tb.Sp 往下走,骨髓脂肪堆积也被压了下去,破骨细胞活性明显减弱。
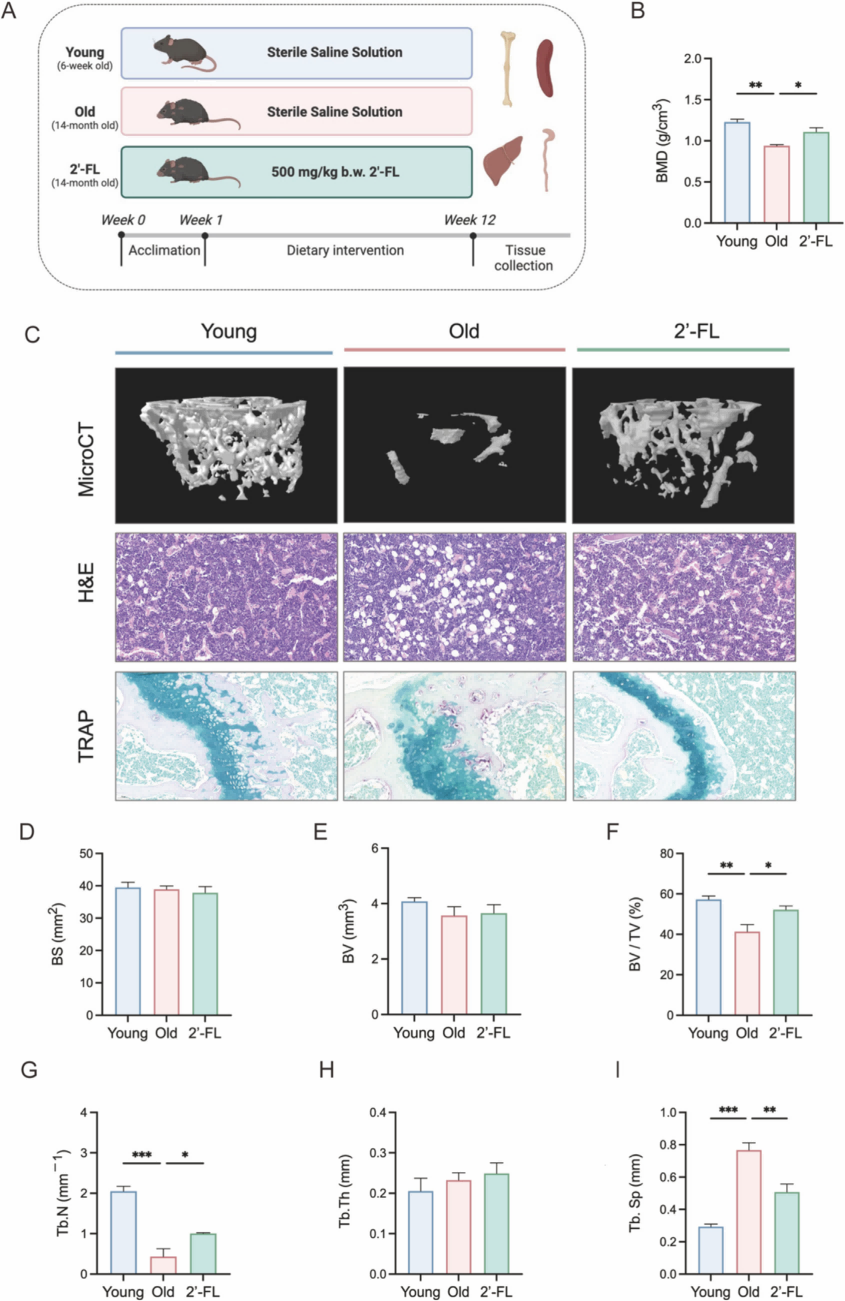
图1 2'-岩藻糖基乳糖(2'-FL)干预恢复老龄相关骨量丢失和骨微结构损伤
03肠道屏障与菌群重塑的作用
整篇工作与当前“健康老龄化”的大背景匹配度很高。现在讨论骨质疏松,越来越多研究把它看成慢性全身炎症和免疫老化的一种表现形式,不再仅仅是单点的骨科问题。作者把 14 月龄小鼠类比中老年人群,从全身炎症、脾脏肿大、骨髓脂肪、骨微结构这些终点切入,把“immunoporosis(免疫性骨质疏松)”这一概念落在看得见的指标上,让读者能直接看到免疫状态失衡、微生态紊乱和骨丢失是怎么叠加在同一只动物身上的。
在肠道层面,文章几乎把近几年“gut–bone axis”的主线跑了一遍。老年小鼠结肠可以看到腺体结构缺失、黏膜溃疡、炎症细胞浸润,紧密连接蛋白 ZO-1 和 Occludin 表达减弱,屏障通透性明显升高。2'-FL 处理后,病理损伤缓解,紧密连接相关 mRNA 和免疫荧光信号恢复到相对健康的水平。
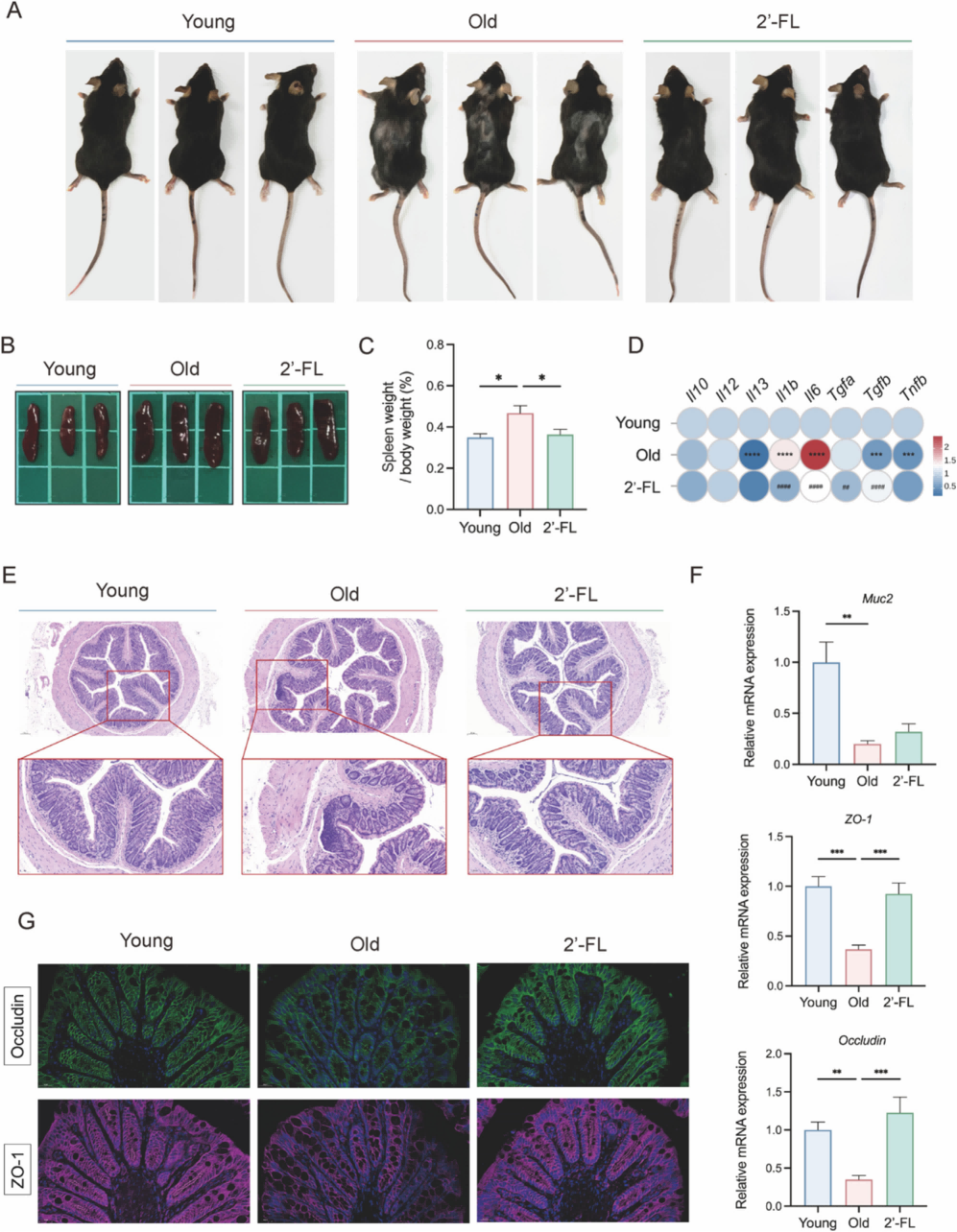
图2 2'-FL 干预缓解老龄相关全身炎症和肠屏障损伤
菌群结果和组织学观察连在一起:老年组 α 多样性下降,Firmicutes/Bacteroidetes 比值抬升,多种与代谢异常、炎症相关的菌属扩张;口服 2'-FL 后,多样性上升,F/B 比值下降,双歧杆菌、乳酸杆菌、Akkermansia、Prevotellaceae 等“友好菌”增多,一些与炎症、代谢紊乱挂钩的细菌被压制。组织病理、屏障蛋白、16S 这一套证据合起来,基本把“2'-FL 能把肠道从偏促炎的状态拉回一个更稳更健康的微生态”这件事交代清楚了。
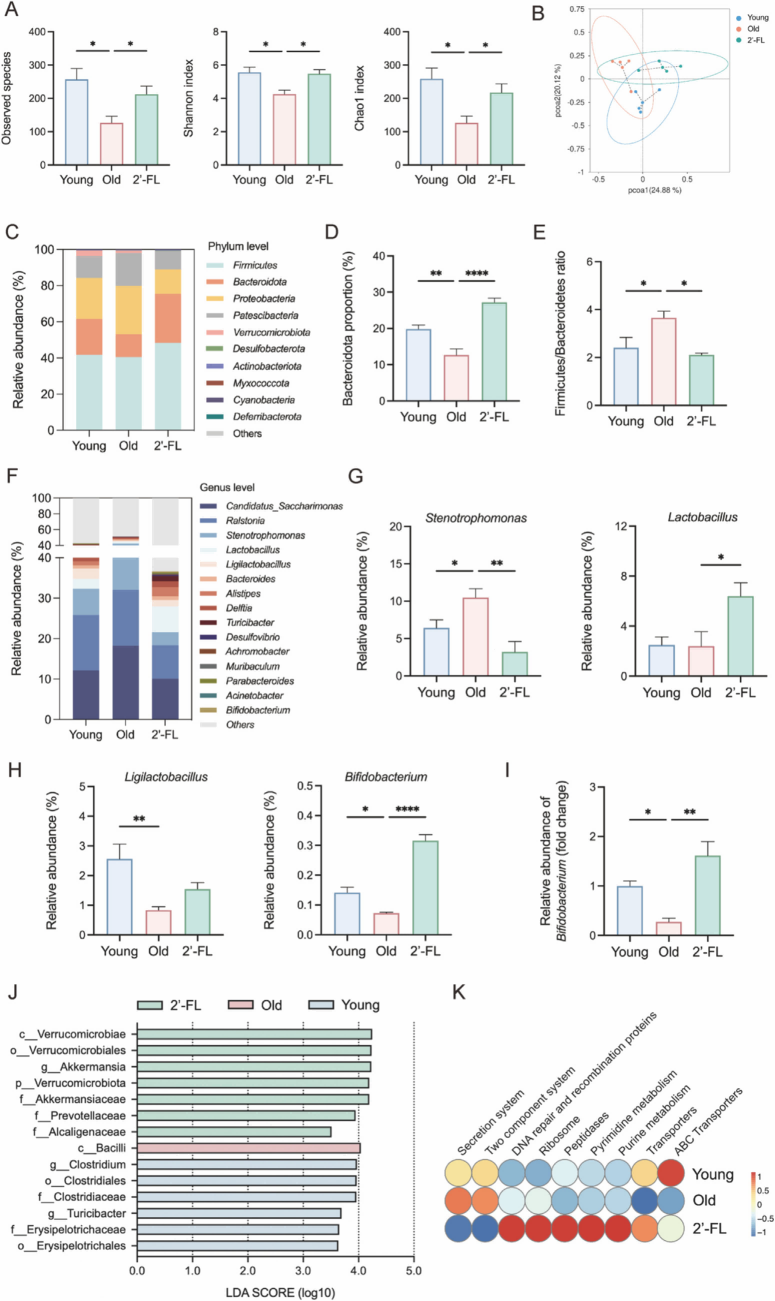
图3 2'-FL 干预调节老龄相关肠道菌群失调
04巨噬细胞 M1/M2 极化重编程
作者没有停留在“炎症指标降低”这一层,而是进一步把视角拉到具体免疫细胞,尤其是巨噬细胞的 M1/M2 极化。在肠系膜淋巴结中,通过流式把树突状细胞亚群和 F4/80⁺CD11b⁺ 巨噬细胞分开看,随年龄增长,免疫细胞构成的确出现偏移,其中最抢眼的是 M1/M2 的失衡:老年组里促炎型 CD86⁺ M1 巨噬细胞比例上升,CD206⁺ M2 下降,M1/M2 比明显偏高,正好对应那种“骨丢失风险持续放大”的免疫背景。加上 2'-FL 之后,M1 比例降下来,M2 回升,M1/M2 比被拉回一个更偏向抗炎和修复的区间,相当于在骨相关免疫微环境中触发了一次“极化重置”。这一步让肠道干预和骨保护之间的链条更加完整。
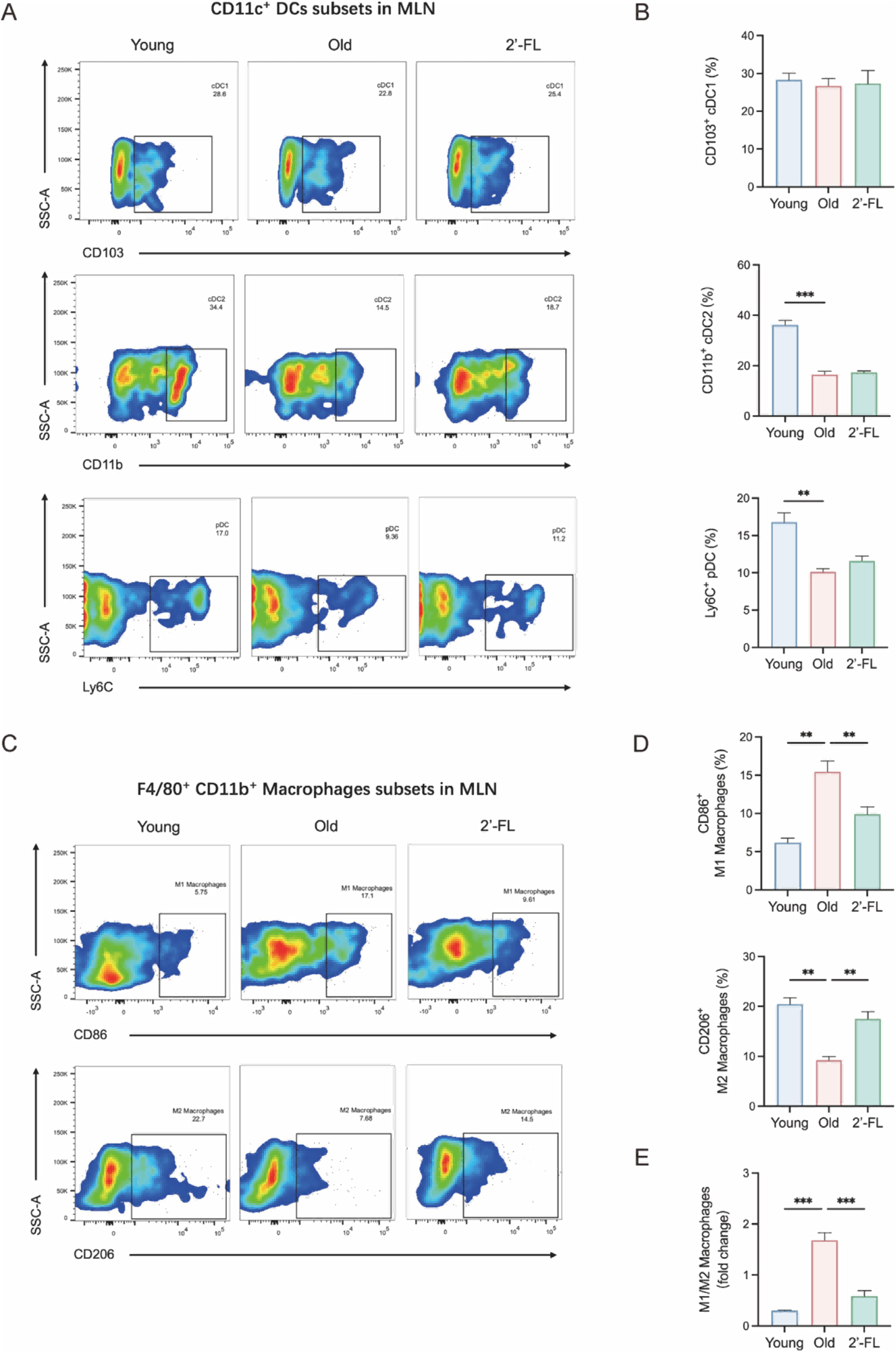
图4 2'-FL 干预调控固有免疫反应
05TLR4/MyD88/NF-κB 轴的机制验证
机制部分选择了现在非常常见也非常“好讲故事”的一条路线:TLR4/MyD88/NF-κB 信号轴。作者在体外用 RAW264.7 细胞搭建 LPS 诱导的 M1 极化模型,先用 CCK-8 把 2'-FL 的安全剂量区间摸清,再看在 LPS 和 2'-FL 共同作用下,M1/M2 极化以及关键信号的变化。LPS 处理之后,M1、M2 都会上升,不过 M1 抬升更明显,整体极化方向偏向促炎;当体系里加上 2'-FL,M1 的比例和一系列标记分子降低,极化状态被往温和方向拉。接下来从基因和蛋白两个层级展开:Tlr4、Myd88、Nfkb1、Il6 等 mRNA 水平均受到 2'-FL 的压制,TLR4、MyD88 以及 NF-κB p65 磷酸化的蛋白信号同步减弱。
更有说服力的一步是加了 TLR4 激动剂,把这把“门锁”强行打开,在这种条件下,2'-FL 对 M1 极化的抑制效果明显减弱,等于用药理学干预确认了这套机制的 TLR4 依赖性。股骨组织里的 TLR4/MyD88/NF-κB 免疫组化染色,则在体内给出了方向一致的结果。从整体动物、到局部组织、到细胞和信号轴,这条链比较清晰地串到了一起。
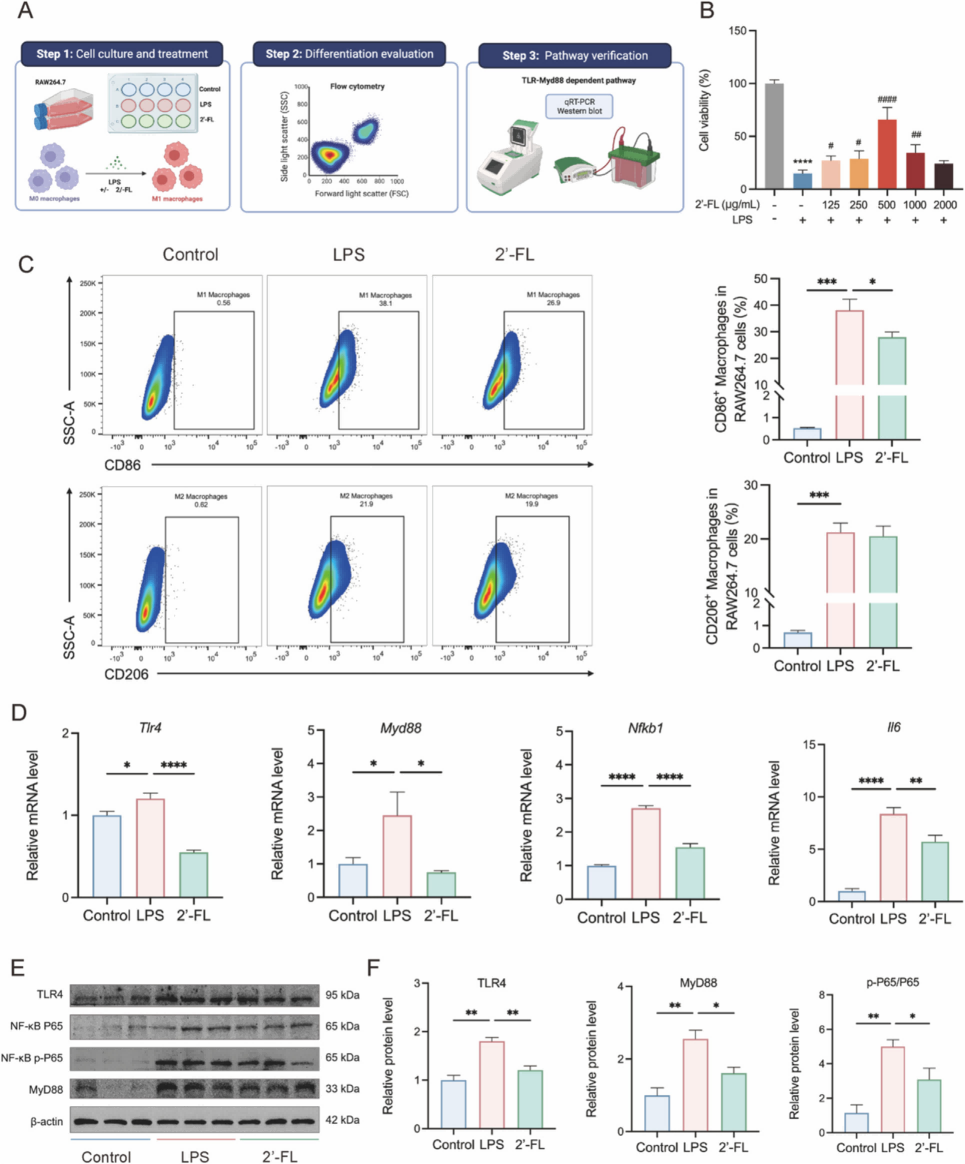
图5 2'-FL 通过靶向 TLR4 及其下游 MyD88/NF-κB 信号通路调节 LPS 诱导的 RAW264.7 巨噬细胞极化
06肠–免疫–骨闭环模型的构建
把前面的结果汇总一下,就能看到一个相对完整、且很方便被后续工作直接复用的“2'-FL–肠–免疫–骨”框架。肠道层面,2'-FL 修补屏障、重建菌群多样性,富集多种与抗炎和代谢健康相关的菌属;免疫层面,通过抑制 TLR4/MyD88/NF-κB 通路,对巨噬细胞极化进行再编程,让系统从偏 M1 的促炎状态回到偏 M2 的修复状态,全身炎症负担降低;骨骼层面,这些变化最终体现在骨密度回升、骨小梁结构恢复、破骨细胞活性降低和骨髓脂肪减少等一整套终点上。对现在大部分做交叉方向的科研人来说,这种“表型–细胞–信号–再回到表型”的闭环非常符合“机制+可转化”的审稿逻辑。
如果再把视角拉宽到整个医学科研和相关产业,2'-FL 在这篇文章里踩中的点其实挺多。健康老龄化让骨质疏松被重新定义成慢性全身炎症和免疫老化的综合后果,单一的补钙或单一抗骨吸收药物越来越难吸引项目资源;肠道微生态研究不断从“谁多谁少”这类描述,向“具体分子+具体靶点”的层级深入,2'-FL 这种结构明确、量产工艺成熟、安全性数据充分的人乳寡糖,非常适合承担“工具分子+潜在产品雏形”双重角色;医用营养和功能食品行业也在寻找下一批“成分明星”,既要有动物和机制支撑,又要有现实的生产和合规路径,而不是无限放大几种传统益生元的边际价值。现在这篇工作相当于把 2'-FL 从“婴幼儿配方中的温和配角”,升级成一个在老年骨质疏松场景下“能够调节肠–免疫–骨轴的候选干预因子”,给了后续选题设计、产品思路和基金申请一套可直接拆用的范本:包括模型的选择,指标组合的搭配,机制做到哪一层算“够用”,证据推理的逻辑。
07对医学科研和转化实践的启示
对做骨代谢、肠道菌群、免疫调节,或者打算进军功能食品与医用营养赛道的团队来说,这篇文章的价值不止在于“告诉你 2'-FL 有效果”,更重要的是已经演示了一条可以照着复刻的路线。前面用自然老龄模型证明 2'-FL 能带来结构层面的骨骼获益,中段用肠道屏障和菌群数据锁定微生态这个起点,再往下通过巨噬细胞极化和 TLR4/MyD88/NF-κB 信号轴拿到先天免疫这一关键中介,最后用体内外多层次结果互相印证。接下来如果想在剂量优化、性别差异、饮食背景、运动联合干预,甚至与其他营养因子联用等方向继续往外扩,这篇文章等于先帮你把底座搭好了。
说简单一点,文章是在用一个很具体的案例说明,当下医学科研可以怎样把微生态、免疫和慢病防治捏成一个有逻辑、有数据、又有转化空间的闭环。这种文章,既方便写综述、写标书,也方便研发团队往产品和方案上做延展。
参考文献:Li A, Kou R, Wang J, Zhang B, Zhang Y, Liu J, Hu Y, Wang S. 2'-Fucosyllactose ameliorates aging-related osteoporosis by restoring gut microbial and innate immune homeostasis. J Adv Res. 2025 Sep;75:651-662. doi: 10.1016/j.jare.2024.11.017. Epub 2024 Nov 14. PMID: 39550028.