CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
本模型以大鼠原代单个心室肌细胞为研究对象,通过Langendorff离体灌流结合酶消化法分离获得活性良好的心肌细胞,再采用全细胞膜片钳技术记录动作电位及离子电流变化,构建细胞水平的心律失常评价体系。
心律失常的发生本质上与心肌细胞膜离子通道功能异常有关,尤其涉及Na⁺电流、Ca²⁺电流及K⁺电流失衡所致的兴奋性、传导性和复极过程异常。因此,本模型通过检测动作电位时程(APD)以及Na⁺、K⁺等跨膜离子电流变化,评价受试药物对异常电生理活动的干预作用。
常以乌头碱等致心律失常因素诱导细胞电生理紊乱,观察药物能否纠正动作电位时程异常延长或缩短、减少异常离子内流或外流,从而判断其潜在抗心律失常活性及可能的作用机制。
SPF级雄性大鼠,体重200~250g。
3%戊巴比妥钠。
正常台氏液、无钙液、Krebs液。
0.05%Ⅱ型胶原酶消化液。
低钠外液、等渗氧化胆碱替代液。
膜片钳电极内液及外液。
乌头碱或其他致心律失常诱导剂。
阳性对照药物,如维拉帕米等。
Langendorff离体心脏灌流装置。
恒温循环系统或恒温水浴装置。
95%O₂+5%CO₂混合供气系统。
倒置显微镜。
膜片钳放大器及全细胞膜片钳记录系统。
微电极拉制仪。
电极三维微操纵器。
灌流系统。
数据采集与分析系统。
计算机及pCLAMP软件。
冰箱或低温保存设备。
常规外科取材器械。
取体重200~250gSPF级大鼠,麻醉后迅速开胸取心脏,行主动脉逆行插管,连接Langendorff灌流装置,以正常台氏液按8mL/min灌流5min,冲洗残余血液。随后改用无钙液灌流约10min,待心脏停止搏动后,再以含0.05%Ⅱ型胶原酶的无钙液继续灌流30min。待心脏质地变软、颜色变浅时,开始分次取心肌组织,每2min取1次。上述操作均在37℃恒温并持续通入95%O₂+5%CO₂条件下进行。
将取下的心室肌组织置于含Krebs液试管中,轻柔吹打分散成单个心室肌细胞,于4℃静置1h备用。挑选杆状、耐钙、横纹清晰、胞质均匀、无明显颗粒样变的心肌细胞用于膜片钳实验。
采用全细胞膜片钳技术记录动作电位及离子电流。将制备好的玻璃微电极充灌电极液,电阻控制在2~3MΩ。将单细胞置于记录浴槽内,以正常台氏液按3mL/min恒速灌流。形成高阻封接(>10GΩ)后,采用负压脉冲打破细胞膜,建立全细胞记录模式,分别在电压钳和电流钳条件下进行刺激与记录。
实验由pCLAMP软件控制并完成数据采集、滤波和存储。记录条件一般在19~22℃下进行。
主要观测指标包括动作电位时程(APD)、Na⁺电流及K⁺电流等。
动作电位时程记录时,采用电流钳模式,在适当保持条件下给予持续2ms、刺激强度80mV的脉冲,诱发单次动作电位,测定APD变化。
Na⁺电流记录时,采用低钠细胞外液,其余以等渗氧化胆碱替代,保持电压为-80mV,从-70mV开始以10mV步阶去极化至+30mV,记录诱发Na⁺内向电流。
K⁺电流记录时,在相应离子隔离条件下,保持电压-80mV,自-40mV开始以10mV步阶去极化至+50mV,刺激持续100ms,间隔10s,记录外向钾电流(以Ito为主)及内向整流钾电流(Ik1)。
实验数据以x±s表示,采用配对t检验分析给药前后动作电位时程及各离子电流变化。
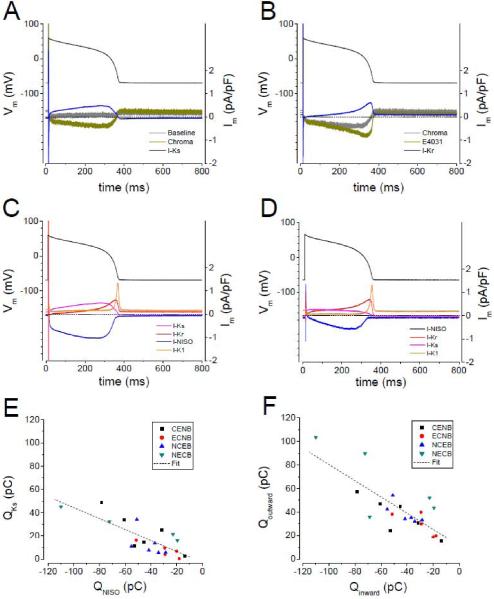
单个心肌细胞动作电位钳及离子电流记录示意图
抗心律失常药物通常根据动作电位时程及离子电流变化进行评价。理想药物本身不应明显缩短正常动作电位时程,但应能纠正致心律失常因素引起的APD异常变化,并改善异常Na⁺或K⁺电流。维拉帕米常可作为阳性对照药物。