CUSTOMER
客户中心
助力生命健康领域从基础研究到产业化的加速转化
2026年度国家自然科学基金医学科学部杰出青年项目的申报窗口临近,许多团队在选题阶段面临一个共性问题:既希望贴近国家重大需求和学科前沿,又不愿陷入概念堆砌与“跟风选题”。在这种背景下,梳理未来数年内医学领域具有持续创新空间和转化潜力的关键方向,具有现实意义。
结合近年来医学杰青立项情况和高水平期刊的研究趋势,可以将当前医学研究的热点与潜在突破口概括为十个板块:
肿瘤精准诊疗与微环境
基因和细胞治疗
免疫与炎症
代谢–心肾疾病
神经科学与脑健康
影像与人工智能
再生医学与组织工程
空间多组学与单细胞
衰老–铁死亡–线粒体稳态
真实世界证据与方法学平台建设
下文围绕这十个方向,尝试从科学问题、技术路径与转化前景三个维度进行系统梳理,供选题与课题设计参考。
一、肿瘤精准诊疗与微环境
肿瘤学仍然是医学杰青最为集中的领域之一,但研究重心正在从“单一靶点”转向“演化过程与时空格局”的综合刻画。一方面,围绕外染色体DNA(ecDNA)、染色体重排等结构变异展开的研究,为理解肿瘤克隆演化、免疫逃逸和治疗耐药提供了新的切入点;另一方面,肿瘤免疫微环境及其空间异质性,借助单细胞多组学与空间转录组技术,正在被系统刻画。
从临床路径看,以循环肿瘤DNA为核心的微小残留病灶(MRD)监测体系,正逐步进入围术期管理和辅助治疗决策。如何在特定实体瘤类型中,将ecDNA/空间异质性等基础研究发现与MRD动态监测结合,建立可验证的风险分层模型和个体化综合治疗策略,是未来几年内极具竞争力的研究方向。
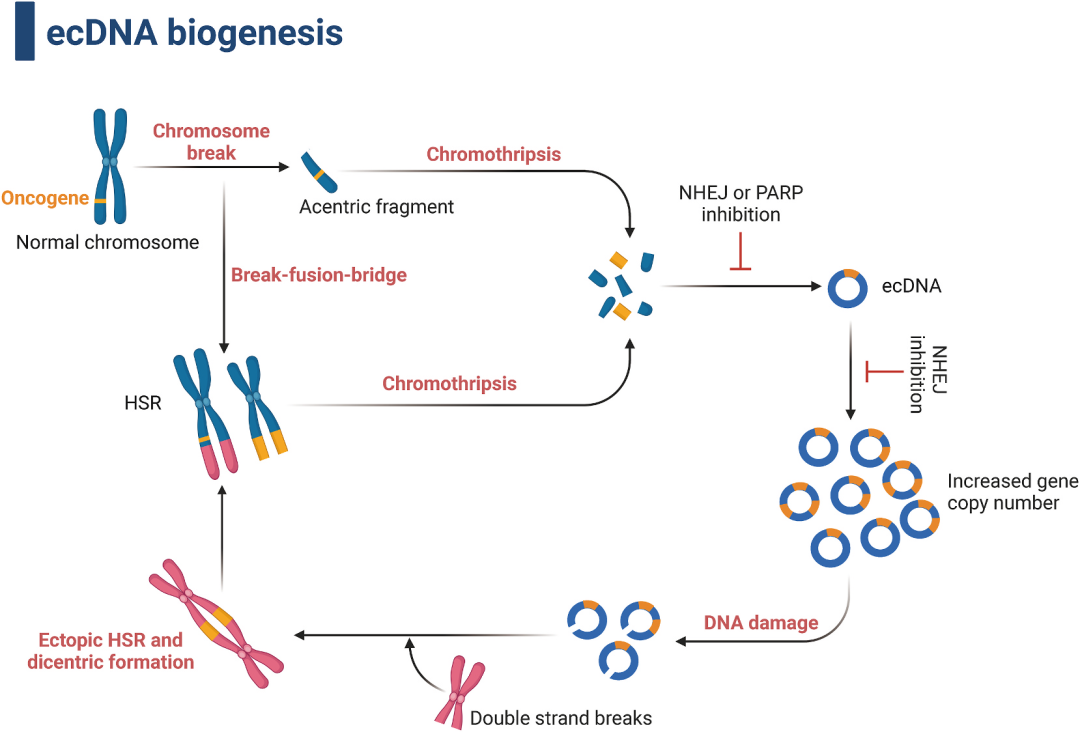
图1. ecDNA生成过程示意图。
二、基因和细胞治疗及递送技术
基因和细胞治疗的发展,使“在体干预遗传与表观遗传信息”成为现实。当前的关键问题不再是单一工具的可行性,而是如何形成“编辑工具–递送系统–安全性评估”三位一体的系统方案。碱基编辑、引导编辑、转座子介导的大片段“写入”、可逆表观编辑等技术,为针对不同疾病的精细调控提供了手段。
同时,脂质纳米颗粒、病毒载体和新型多组分纳米递送系统的发展,使器官选择性和细胞类型选择性成为可设计参数。在线粒体疾病、遗传代谢病、造血系统疾病以及部分肿瘤中,如何在体内实现高效、可控、可随访的基因/细胞治疗,如何规范地评估长期安全性与免疫原性,将是该板块的重要方向。与此相配套的,是个体化mRNA疫苗、CAR-NK/CAR-M等细胞产品在实体瘤和感染性疾病中的应用优化问题。
三、免疫与炎症
免疫学研究正在从局限于单一细胞亚群或通路的描述,扩展为跨时间、跨器官的系统性分析。训练免疫、免疫代谢重编程、乳酸化修饰、SASP及细胞焦亡等概念,构成了一套彼此关联的理论框架。例如,在动脉粥样硬化、慢性感染和肿瘤发生发展过程中,先天免疫细胞代谢与表观遗传状态的长期重构,可能决定疾病进程与治疗响应。
在适应性免疫方面,T 细胞衰竭的发生、逆转及持久记忆形成,与能量代谢、酸碱微环境密切相关;在衰老相关研究中,不同谱系细胞的SASP特征及其对组织稳态和免疫微环境的影响,为“选择性清除衰老细胞”的干预策略奠定基础。结合微生物组–免疫–代谢三者之间的因果关系解析,未来有望在动脉粥样硬化、自身免疫疾病、肿瘤免疫治疗应答等场景中,提出更具针对性的干预策略。
四、代谢–心肾–全身性疾病
在代谢及心肾疾病领域,新一代降糖和心肾保护药物的临床结果,已经明显改变了疾病防治格局。研究不再停留于“是否有效”,而是转向“如何在合适的人群中,以合适的时机和组合方式使用”。围绕GLP-1 受体激动剂以及多重受体激动剂的多器官保护机制,系统分析炎症、免疫和代谢通路之间的交织,是重要方向之一。
此外,以Lp(a)、残余炎症风险、脂蛋白亚型等为核心变量的心血管风险再分层,也需要更多机制性和随访研究予以支撑。在慢性肾脏病、尤其是糖尿病肾病中,将组学数据、循环生物标志物与长期结局相结合,构建预测进展与药物获益的模型,有望推动个体化治疗策略的形成。整体而言,该板块更强调“多器官共病”的系统视角和长期随访数据的整合应用。
五、神经科学与脑健康
神经系统疾病研究的趋势,可以概括为三个关键词:清除系统、结构连接和易感性。首先,脑–淋巴及类淋巴清除系统的功能,尤其是其与睡眠节律的关系,被认为与蛋白聚集、代谢废物积累及神经退行性疾病早期病理密切相关。如何在动物模型和人群研究中准确量化这一系统的功能,是当前的一个难点。
其次,人脑类器官与组装体技术的进展,使跨脑区、跨层级的连接重塑在体外模型中得到模拟,为复杂神经疾病机制和用药反应提供了新平台。
第三,情绪障碍、应激相关疾病和认知障碍中的个体易感性,越来越多地被放在“免疫–代谢–神经”耦合网络中去理解。通过队列数据、多模态影像与类器官/动物模型之间的互相印证,有望构建更为完整的病程进展图谱。
六、医学影像与人工智能
医学影像正在从定性描述转向定量和推断导向。以全身PET/CT、PCD-CT 为代表的新一代成像技术,为多器官功能评估、药物分布和疗效监测提供了更精细的数据基础。从研究视角看,关键不在于单一成像序列或设备,而在于如何基于影像构建可重复、可解释的量化指标体系,并与临床终点、组学特征相衔接。
在人工智能方面,跨模态基础模型(如影像–病理–空间组学的联合建模)、眼底图像基础模型在全身性风险预测中的应用等,已经展示了“单一模态推断系统性疾病风险”的可能性。围绕这些模型开展的工作,不仅包括模型本身的性能和泛化能力,还需要关注公平性、可解释性以及在具体疾病管理流程中的嵌入方式。
七、再生医学与组织工程
再生医学与组织工程领域的一个显著变化,是评价标准从“是否可以构建组织/器官”转向“是否具备可规模化制备和可量化功能评估能力”。免疫兼容、血管化的类器官与器官芯片,是当前重点关注的方向之一。这类模型不仅可用于基础研究,还可用于个体化用药筛选和毒性评估,对接临床转化场景。
同时,以可降解或智能响应材料为载体,设计细胞因子和生物活性分子的时序释放,实现对组织修复过程的程序化调控,是另一重要问题。借助高分辨率影像和功能测定,对再生过程进行连续监测和定量分析,有助于提高再生干预策略的可控性和可重复性。
八、空间多组学与单细胞
空间多组学与单细胞技术已成为研究组织结构、细胞通讯和微环境重塑的核心方法,但其真正价值取决于是否能形成“技术平台+生物学问题”的有机结合。一方面,建立从样本获取、预处理、测序到数据分析的标准化流程,并配套相应的算力与软件平台,是实现大规模应用的前提;另一方面,在具体疾病场景下,如何通过多维数据整合,提出可验证的关键通路和干预靶点,是评估研究价值的关键。
在实体瘤、自身免疫疾病、组织纤维化和发育异常等领域,空间分辨率和细胞类型解析能力的提升,使研究者有机会从更细致的视角理解病变的起点、扩展路径和潜在逆转窗口。
九、衰老、铁死亡与线粒体稳态
衰老相关研究与铁死亡、线粒体功能的交汇,构成了贯穿多种慢性疾病的基础科学问题。衰老相关分泌表型(SASP)的细致解析,有助于识别在不同组织和疾病背景中发挥主导作用的细胞群体与信号网络,从而为选择性清除或调控衰老细胞提供依据。铁死亡及脂质过氧化在肿瘤治疗中的作用,尤其是与放疗、免疫治疗的协同效应,是药物设计和组合方案优化的重要理论基础。
线粒体–核基因组互作对细胞命运决策、应激反应和疾病易感性的影响,是另一条值得关注的主线。通过单细胞、多组学和功能实验结合,解析不同细胞状态下线粒体稳态失衡的模式,有望为慢性炎症、代谢性疾病、神经退行性疾病甚至肿瘤提供新的干预视角。
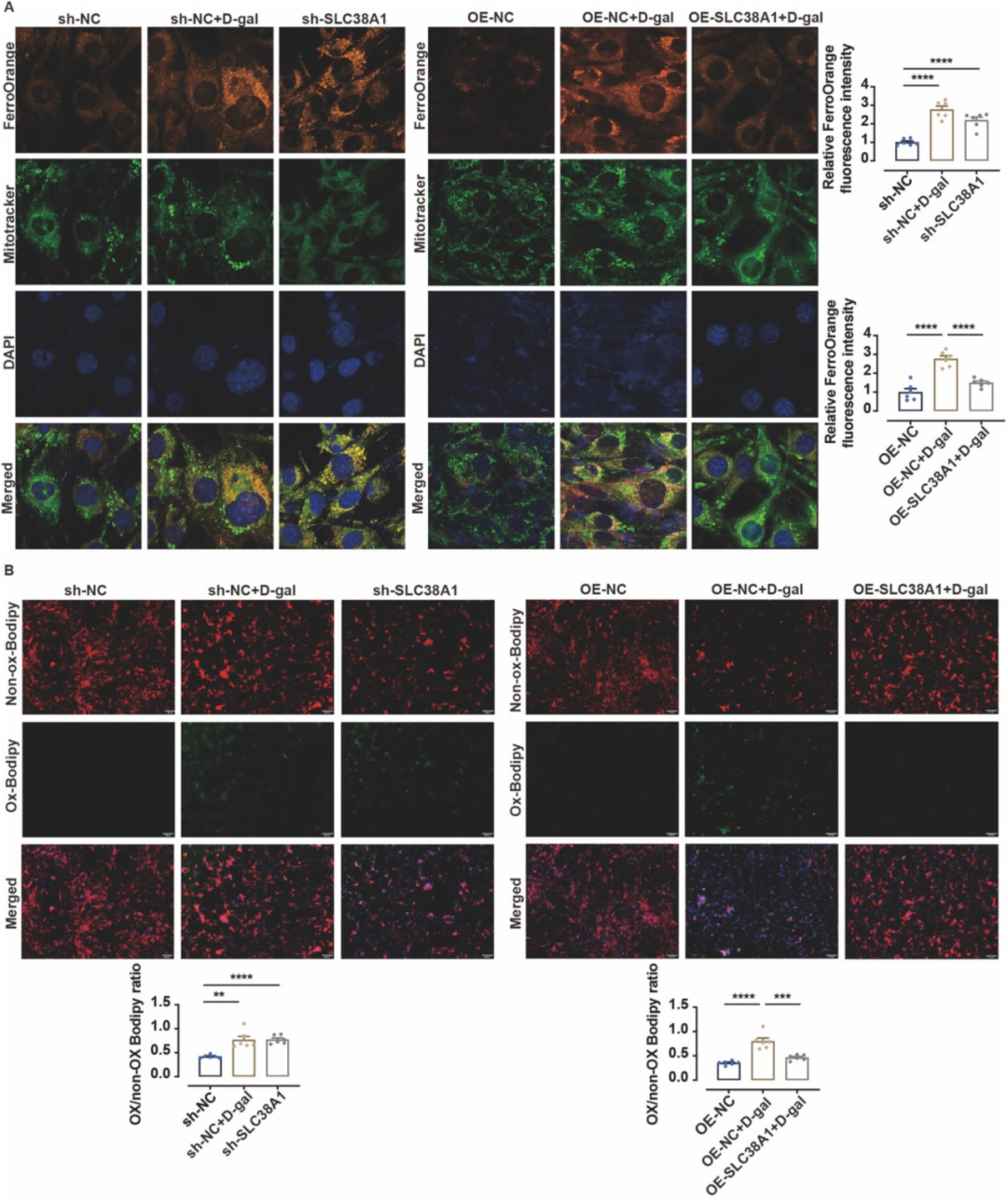
图2. SLC38A1在D-gal处理的C2C12细胞中发挥保护作用,减轻铁过载和脂质过氧化。
十、真实世界证据与方法学平台建设
最后,一个独立但高度交叉的方向,是围绕大规模生物样本库、专病队列和临床数据库,构建规范化的真实世界证据平台,并在此基础上发展适用于医学研究的统计与因果推断方法。与传统随机对照试验相比,真实世界数据更贴近临床实践,但同时也存在偏倚多、数据异质性强等问题。如何通过严谨的设计和分析方法,尽可能减少混杂和选择偏倚,是方法学研究的重要任务。
在肿瘤、心血管、肾脏、内分泌和神经系统疾病等领域,若能将影像、多组学、实验室指标、治疗过程和长期结局进行系统整合,并在此基础上构建规范的数据治理与分析框架,将为新型诊疗策略的评价和推广提供坚实支撑。对于具备队列建设和数据平台基础的团队而言,这一方向既可作为独立研究主题,也可以为其他九个板块提供共同的研究基础设施。
结语
从上述十大方向可以看到,2026年国自然医学杰青的选题空间并不狭窄,但真正具有说服力的课题,往往具备三个特征:
(1)聚焦明确的疾病场景与人群;
(2)依托一到两类自身掌握较好的关键技术平台;
(3)可量化且具有实际临床或转化意义的结局指标。
在此基础上,再考虑如何在机制阐明、方法学创新和转化路径之间建立清晰的逻辑联系,往往比单纯追逐某个“热点词”更为关键。